- نحوه ی دسترسی به پایان نامه های دانشگاه های مختلف جهان
- کاغذ لیتموس برای شناسایی غذاهای فاسد
- وجود سلنیم در خون مادر از ورود سم به بدن جنین جلوگیری میکند
- تعادل شیمیایی-شیمی تجزیه
- اثزدما بر تعادل-شیمی تجزیه رشته صنایع شیمیایی
- اثر دما بر انحلال پذیری-شیمی تجزیه رشته صنایع شیمیایی
- آدرس فیسبوک سایت
- چگونه برف درست کنيم
- دودزا
- نارنجک با پرمنگنات پتاسيم
آخرین مطالب
کشف پرتو زایی عناصر پرتو زا (رادیو اکتیو)
توریم و اورانیوم و بعضی از عناصر دیگر بدون هیچ اثر خارجی (یعنی به سبب عوامل داخلی) پیوسته تابش مرئی گسیل می دارند. این تابش مانند اشعه ایکس به درون حائل های کدر نفوذ می کند. و روی فیلمهای عکاسی اثر می گذارد. و اثر یونشی به وجود می آورد
● کشف پرتو زایی عناصر پرتو زا (رادیو اکتیو) توریم و اورانیوم و بعضی از عناصر دیگر بدون هیچ اثر خارجی (یعنی به سبب عوامل داخلی) پیوسته تابش مرئی گسیل می دارند. این تابش مانند اشعه ایکس به درون حائل های کدر نفوذ می کند. و روی فیلمهای عکاسی اثر می گذارد. و اثر یونشی به وجود می آورد. ویژگی گسیل خود به خودی چنین تابش به پرتوزایی معروف است به عناصر دارای این ویژگی عناصر رادیو اکتیو می گویند و تابشی که این عناصر گسیل می دارند تابش پرتوزایی (تشعشع هسته ای) نامیده می شود. خاصیت پرتوزایی اورانیم را در سال ۱۸۹۶ آنتوان هانری بکرل فیزیکدان فرانسوی کشف کرد. پرتوزایی اندکی پس از کشف اشعه ایکس کشف شد.
▪ عناصر رادیو اکتیو محصول آزمایشات اولیه: گسیل پرتوهای ایکس اولین بار در بمباران دیواره های شیشه ای لامپ تخلیه گازی با پرتوی کاتدی کشف شد. موثرترین نتیجه این بمباران تابانی شدید شیشه به رنگ سبز یعنی لیانی است. از اینجا معلوم می شود پرتوهای ایکس حاصل لیانی است و با هر لیانی همراهند، از جمله موردی که با نور برانگیخته شود. بکرل این فرض را از راه آزمایش تحقیق کرد او مواد لیان را در معرض نور قرار داد و آن گاه این مواد را کنار فیلم عکاسی که در لفاف سیاه پیچیده شده بود، قرارداد. پس از ظاهر کردن فیلم عکاسی گسیل تابش نفوذی را از روی سیاه شدن فیلم آشکار ساخت. از میان تمام مواد لیان که توسط بکرل مورد آزمایش قرارگرفت فقط نمکهای اورانیوم صفحه عکاسی را سیاه کردند. با وجود این معلوم شد که نمونه ای که قبلا در معرض تابش نور شدید قرارگرفته باشد به همان اندازه نمونه ای که برانگیخته نشده باشد، صفحه عکاسی را سیاه می کند. از این مشاهده چنین استنباط می شود که گسیل تابش توسط نمک اورانیم به لیانی مربوط نیست و به اثرهای خارجی بستگی ندارد. این نتیجه با آزمایش هایی که با ترکیبهای محتوی غیر لیان که همه تابش نفوذ کننده گسیل می دارند انجام شد و مورد تایید قرارگرفت.
▪ سیر تحولی و رشد: بعد از کشف خاصیت پرتوزایی اورانیوم توسط بکرل ، ماری کوری فیزیکدان فرانسوی متولد لهستان که بیشترین تحقیقات خود را همراه با شوهرش پیر کوری انجام داد بیشتر عناصر شناخته شده و خیلی از ترکیبها را مورد بررسی قرارداد. تا ببیند که آیا آنها خاصیت پرتوزایی دارند یا خیر. ماری کوری در آزمایشهایش یونش هوا را به عنوان شاخص خاصیت پرتوزایی مواد پرتو زا به کار می برد. این روش خیلی حساستر از روش مبتنی بر تاثیر روی صفحه عکاسی است. آزمایشهای ماری کوری به نتایج زیرمنتهی شد.
▪ نتایج آزمایشات ماری کوری: پرتوزایی نه فقط در اورانیوم بلکه در همه ترکیبات شیمیایی آن مشاهده می شود. افزون بر آن خواص پرتوزایی در مورد توریم و همه ترکیبات شیمیایی آن نیز وجوددارد. پرتوزایی نمونه ای از هر ترکیب شیمیایی اورانیوم و توریم برابر است با پرتوزایی اورانیم و توریم خالص موجود در آن ترکیب نتیجه اخیر نشان می دهد که خواص مولکول موجود در عنصر پرتوزا روی خاصیت پرتوزایی موثرنیست. بنابر این پرتوزایی خاصیت ذاتی اتمهای عنصرپرتو زا است نه پدیده مولکولی. علاوه بر عناصر خالص و ترکیبات آنها ماری کوری تعدادی از سنگهای معدنی را نیز بررسی کرد. و معلوم شد که پرتوزایی کانیها از حضور اورانیم و توریم در آنها ناشی می شود با وجود این خاصیت پرتوزایی بعضی از کانیها به طور غیر قابل انتظار خیلی بالاست. برای مثال پیچ بلند چهار برابر مقدار اورانیم موجود در خود یونش نشان می دهد. پرتوزایی بالای پیچ بلند را فقط می شد به عنصر پرتوزای ناشناخته موجود در این مقدار کم نسبت داد که تحلیل شیمیایی نتوانسته بود وجود آن را آشکار سازد. به رغم مقدار کم آن شار تابشی که این عنصرگسیل می کرد، قویتر از اورانیم موجود در یک مقدار بزرگتر بود. بنابراین پرتوزایی این عنصر باید چند برابر شدیدتر از پرتوزایی اوارنیم باشد. در نتیجه این ملاحظات ، پیر و ماری کوری کوشش کردند این عنصر فرضی را به طور شیمیایی از پیچ بلند جدا کنند. پرتوزایی به ازای واحد جرم محصول نهایی نشانه ای از توفیق در عملیات شیمیایی بود. این مقدار باید با افزایش مقدار عنصر جدید در محصول نهایی افزایش می یافت. پس از سالها کار سخت آنها سرانجام توفیق یافتند چند دهم از عنصرخالص به دست آورند که خاصیت پرتوزایی آن بیش از میلیون برابر اورانیوم بود. این عنصر به رادیوم یعنی تابان معروف است.
▪ عنصر رادیو اکتیو رادیوم: رادیم بنا به خواص شیمیایی آن یک فلز قلیایی خاکی است. برای جرم اتمی آن عدد ۲۲۶ به دست آمد با توجه به خواص شیمیایی و جرم رادیوم در خانه خالی ۸۸ جدول تناوبی قرارداده شد. در سنگهای معدنی اورانیم همیشه رادیوم به مقدار خیلی کم وجود دارد (حدود ۱ گرم رادیوم در ۳ تن اورانیوم). به این سبب استخراج رادیوم فرایند پرزحمتی است. رادیوم یکی از فلزات کمیاب و بسیار گرانبهاست. و به عنوان چشمه متمرکز تابش پرتوزا ارزش زیادی دارد. ▪ سایر عناصر رادیواکتیو: تحقیقات بعدی که توسط کوریها و دیگر دانشمندان انجام گرفت شمار عناصر پرتوزای شناخته شده را به مقدار زیادی افزایش داده است. معلوم شده است که تمام عناصری که عدد اتمی آنها بیش از ۸۳ باشد، پرتوزا هستند. معمولا این عناصر را به مقدار کم از آمیزه های اورانیوم ، رادیوم و توریم به دست آوردند. ایزوتوپهای پرتوزای تالیم ، سرب و بیسموت نیز از طریق مشابه پیدا شدند. باید توجه داشت که فقط ایزوتوپهای کمیاب این عناصر که با اورانیم ، رادیم و توریم آمیخته باشند، پرتوزا هستند. تالیم ، سرب و بیسموت معمولی پرتوزا نیستند. افزون برعناصر آخر جدول تناوبی ، معلوم شده است که ساماریوم ، سزیم و روبیدیوم نیز پرتوزا هستند. پرتوزایی این عناصر ضعیف و با زحمت آشکارسازی می شود.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 298 تاريخ : سه شنبه تير 1388 ساعت: 20:9
Heat Transfer (J.P. Holman).rar
Click here to download this file
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 454 تاريخ : سه شنبه تير 1388 ساعت: 14:9
ارزیابی اختصاصات مخزنی شامل مطالعه پارامترهای پتروفیزیکی نظیر تخلخل، نفوذپذیری و اشباع سیالات؛ تغییرات لیتولوژیکی نسبت به عمق و اختصاصات هیدروکربنی از جمله ضخامت مفید، غیرمفید و ستون مفید هیدروکربوری است. سنگهای کربناته همراه با ماسه سنگها، سنگهای مخزنی نفت و گاز عمده ای را در دنیا تشکیل می دهند. مخزن آسماری میدان نفتی منصوری از جمله مخازن کربناته ترشیری ایران است که در ۴۰ کیلومتری جنوب اهواز قرار دارد. این مخزن به ۸ زون تقسیم شده که هر زون دارای لیتولوژی و اختصاصات پتروفیزیکی مربوط به خود است. با توجه به اینکه در مخزن آسماری میدان منصوری هر سه لیتولوژی عمده مخازن (ماسه سنگ، سنگ آهک و دولومیت) وجود دارد، مطالعه لیتولوژی و تاثیر آنها بر پارامترهای پتروفیزیکی مخازن از اهمیت زیادی برخوردار است. بررسی مقاطع نازک و نمودارهای چاه پیمایی حاکی از آن است که زون یک عمدتا کربناته (آهکی و دولومیتی)، زونهای ۲، ۳،۴ و ۵ عمدتا ماسه سنگی (بخش ماسه سنگی اهواز)، زون ۶ مخلوطی از سنگ آهک، دولومیت، ماسه و شیل و زونهای ۷ و ۸ آهکی و شیلی است. بر اساس ارزیابی های به عمل آمده زون ۲ با بیش از ۸۰ درصد ماسه بیشترین ستون مفید هیدروکربنی، ضخامت خالص و نسبت ضخامت خالص به کل را دارا بوده و نظر به اشباع آب کم آن (حدود ۲۰ درصد برای زون های مفید)، بهترین کیفیت مخزنی را در بین زون های دیگر دارا می باشد. پس از آن زون های ۳ و ۱ از کیفیت مخزنی مناسب تری برخوردارند. از آنجایی که زونهای ۴ تا ۸ زیر سطح تماس آب و نفت قرار دارند، زون تولیدی نبوده و از کیفیت مخزنی پایینی برخوردارند. زون ۲ بهترین لایه تولیدی نفت از نظر پارامترهای پتروفیزیکی به شمار می رود.
ارزیابی اختصاصات مخزنی شامل مطالعه پارامترهای پتروفیزیکی نظیر تخلخل، نفوذپذیری و اشباع سیالات؛ تغییرات لیتولوژیکی نسبت به عمق و اختصاصات هیدروکربنی از جمله ضخامت مفید، غیرمفید و ستون مفید هیدروکربوری است. سنگهای کربناته همراه با ماسه سنگها، سنگهای مخزنی نفت و گاز عمده ای را در دنیا تشکیل می دهند. مخزن آسماری میدان نفتی منصوری از جمله مخازن کربناته ترشیری ایران است که در ۴۰ کیلومتری جنوب اهواز قرار دارد. این مخزن به ۸ زون تقسیم شده که هر زون دارای لیتولوژی و اختصاصات پتروفیزیکی مربوط به خود است. با توجه به اینکه در مخزن آسماری میدان منصوری هر سه لیتولوژی عمده مخازن (ماسه سنگ، سنگ آهک و دولومیت) وجود دارد، مطالعه لیتولوژی و تاثیر آنها بر پارامترهای پتروفیزیکی مخازن از اهمیت زیادی برخوردار است. بررسی مقاطع نازک و نمودارهای چاه پیمایی حاکی از آن است که زون یک عمدتا کربناته (آهکی و دولومیتی)، زونهای ۲، ۳،۴ و ۵ عمدتا ماسه سنگی (بخش ماسه سنگی اهواز)، زون ۶ مخلوطی از سنگ آهک، دولومیت، ماسه و شیل و زونهای ۷ و ۸ آهکی و شیلی است. بر اساس ارزیابی های به عمل آمده زون ۲ با بیش از ۸۰ درصد ماسه بیشترین ستون مفید هیدروکربنی، ضخامت خالص و نسبت ضخامت خالص به کل را دارا بوده و نظر به اشباع آب کم آن (حدود ۲۰ درصد برای زون های مفید)، بهترین کیفیت مخزنی را در بین زون های دیگر دارا می باشد. پس از آن زون های ۳ و ۱ از کیفیت مخزنی مناسب تری برخوردارند. از آنجایی که زونهای ۴ تا ۸ زیر سطح تماس آب و نفت قرار دارند، زون تولیدی نبوده و از کیفیت مخزنی پایینی برخوردارند. زون ۲ بهترین لایه تولیدی نفت از نظر پارامترهای پتروفیزیکی به شمار می رود.
Evaluation of reservoir characteristics and lithology of Asmari formation in Mansuri oil field By: Saeid Alizadeh Pirzaman Abstract Evaluation of reservoir characteristics includes petrophysical parameters like Porosity, Permeability and fluid saturations, net thickness, net to Gross ratio and oil column and lithologic variations versus depth. Asmari Reservoir of Mansuri oil field is one of the Tertiary Carbonate reservoirs of Iran which is located 40 km south to Ahwaz city. This reservoir is divided into 8 zones. Each zone has special lithology and petrophysical properties. Zone 1 is generally carbonate (limestone and dolomite), zones 2, 3, 4 and 5 sandy (Ahwaz sand member), zone 6 mixture of Sandstone, limestone, dolomite and shale and zones 7 & 8 limestone and shale.
Based on the petrophysical evaluations zone 2 (by more than 80 percent sand) is the best pay zone and has the most values of net thickness, net to gross ratio and oil column and oil saturation. Also this paper shows that zones 3 and 1 follow the zone 2 respectively. Zones 4 to 8 are located below the oil water contact and are not pay zones.
مقدمه
هدف اصلی اختصاصات مخزنی، بازسازی اختصاصات پتروفیزیکی نظیر تخلخل، نفوذپذیری و اشباع سیالات می باشد. نحوه توزیع تخلخل می تواند رابطه متداول میان این اختصاصات باشد. در این ارتباط نمودارهای چاه پیمائی ابزار مناسبی است [۴]. ارتباط بین اختصاصات پتروفیزکی و زمین شناسی (لیتولوژی) موضوعی بوده که از سال ۱۹۵۵ تا کنون شدیداً مطالعه شده است. تخلخل و نفوذپذیری لایه کربناته ناشی از واکنش میان انواع مواد اولیه رسوب و تنوعی از فرآیندهای دیاژنتیکی است.
نمودارهای چاه پیمائی ثبت پیوسته ای از پارامترهای سازنده نسبت به عمق را بدست می دهد که کاربرد زمین شناسی بسیار مفیدی دارد [۸]. ترکیب سازندها به کمک نمودارهای چاه پیمائی (نظیر دانسیته، نوترون و اشعه گاما) می تواند بصورت کانی و یا عناصر شیمیائی بیان شود و بنابراین میان پارامترهای پتروفیزیکی و ترکیب سنگ رابطه وجود دارد. اطلاعات حاصل می تواند منجر به تفسیر بهتر جهت اکتشاف و تولید و لذا اختصاصات پیشرفته مخزن شود [۲].
سنگهای کربناته همراه با ماسه سنگها، سنگهای مخزنی نفت و گاز عمده ای را در دنیا تشکیل می دهند. ذخایر هیدروکربن در این سنگها اساسا با دولومیت همراه است [۹ & 3]. دولومیت ها حدودا %۳۰ مخازن کربناته جهان را شامل می شوند و تقریبا۸۰ درصد نفت و گاز قابل استحصال سنگهای کربناته آمریکای شمالی را در خود جای داده اند [۱۳]. دوسوم نفت خاورمیانه در کربناتها جای گرفته و مخازن آسماری ایران با سن الیگومیوسن (ترشیری) در زمره مخازن دولومیتی نیز ذکر شده است [۱۱]. این نوع مخازن نسبت به مخازن کلاستیکی (به عنوان مثال ماسه سنگها) بسیار هتروژن است [۹]. به عنوان مثال با افزایش عمق، دولومیت ها مخازن بهتری را نسبت به سنگهای آهکی ایجاد می کنند. با توجه به اینکه در مخزن آسماری میدان منصوری هر سه لیتولوژی عمده مخازن (ماسه سنگ، سنگ آهک و دولومیت) وجود دارد، مطالعه لیتولوژی و تاثیر آنها بر پارامترهای پتروفیزیکی مخازن از اهمیت زیادی برخوردار است.
این موضوع اساسا به محیط رسوبگذاری رخساره های متعدد، فرایندهای تکتونیکی و دیاژنتیکی (سیمانی شدن، دولومیتی زاسیون، تبلور مجدد، شکستگی و …) مربوط است که سنگهای کربناته را همراهی می کند [۶&10]. بعلاوه شکستگی نیز نقش مهمی را در مخازن ایفا میکند و تخلخل و نفوذ پذیری ایجاد شده، آنیزوترپی عمده ای را در مخزن [۷ & 9] بوجود می آورد. لذا، مطالعه لیتولوژی های مختلف و تاثیر آنها بر پارامترهای پتروفیزیکی مخازن از اهمیت زیادی برخوردار است[۵].
میدان نفتی منصوری
میدان نفتی منصوری در ۴۰ کیلومتری جنوب شهر اهواز واقع است و فاقد هر گونه ساختمان سطحی بوده و اساسا ساختاری است که به وسیله لرزه نگاری مشخص شده است. این میدان در سال ۱۳۴۱ اکتشاف گردیده و دارای چند سازند مخزنی (سازند آسماری و بخش ماسه سنگی اهواز، سازند ایلام و سازند سروک است). این میدان از سال ۱۳۵۳ مورد بهره برداری قرار گرفت و تا خرداد ۱۳۸۳ تعداد ۵۸ حلقه چاه در آن حفاری گردیده است. بر اساس نقشههای حاصل از مطالعات لرزهنگاری و نقشههای ساختمانی زیرزمینی تهیه شده، میتوان میدان منصوری را تاقدیسی کشیده با دامنههای ملایم و کم شیب در راستای شمال غرب ـ جنوب شرق در نظر گرفت. شیب دامنه شمالی کمی بیشتر از دامنه جنوبی است و به ترتیب حدود ۸-۶ درجه و ۶-۵ درجه شیب دارند. شیب دماغههای شرقی و غربی نیز حدود ۱ تا ۵/۱ درجه میباشد.
مخزن آسماری و بخش ماسهسنگی اهواز حاوی نفتی با ۳۰ درجة API و ۲ درصد سولفور است ]۱[. ابعاد مخزن آسماری در سطح تماس آب و نفت حدود ۳۰ کیلومتر طول و ۵/۳ کیلومتر عرض دارد. سطح تماس آب و نفت در این مخزن در حدود عمق ۲۲۷۲ متری زیر سطح دریا تعیین شده است. با توجه به اینکه نقطة ستیغ مخزن بر روی نقشه ساختمانی حدود عمق ۲۱۴۴ متری زیر سطح دریا را نشان میدهد و با احتساب آخرین منحنی بسته مخزن (۲۴۰۰ متری)، میزان بستگی قائم در حدود ۲۵۶ متر محاسبه شده است، ارتفاع ستون نفت در قسمتهای مرکزی مخزن حدود ۱۲۸ متر میباشد که به سمت دماغههای مخزن از میزان آن کاسته میشود.
بحث
لیتولوژی:
بررسیهای پتروگرافی مقاطع نازک و مطالعات نمودارها حاکی از آن است که مخزن آسماری در این میدان تناوبی از آهک، دولومیت، ماسه سنگ و شیل است. مخزن آسماری به ۸ زون (لایه) تقسیم شده و هر زون دارای لیتولوژی و اختصاصات پتروفیزیکی مربوط به خود است. زون ۱ عمدتا کربناته (آهکی و دولومیتی)، زونهای ۲،۳،۴ و ۵ عمدتا ماسه سنگی (بخش ماسه سنگی اهواز)، زون ۶ مخلوطی از سنگ آهک، دولومیت، ماسه و شیل و زونهای ۷ و ۸ آهکی و شیلی است. اشکال ۱ و۲ درصد ماسه، دولومیت آهک و رس موجود در زون های مختلف چاه شماره ۴۶ این میدان را نشان می دهد.
پارامترهای پتروفیزیکی:
مخزن آسماری در میدان منصوری به ۸ زون تقسیم بندی شده است. زونهای ۱، ۲ و ۳ حاوی هیدروکربن بوده و بقیه زونها اشباع از آب می باشند. زون ۲ این مخزن کیفیت مخزنی محسوسی نسبت به بقیه زون ها دارد. در شکل ۲ تعدادی از نمودارهای ارزیابی پارامترهای پتروفیزیکی مخزن برای چاه شماره ۴۶ منصوری و در شکل ۳ برای زون ۲ کل میدان جهت نمونه آورده شده است. ارزیابی پتروفیزیکی این زون ها به شرح زیر است:
زون۱- این لایه عمدتاً از آهک های دولومیتی و دولومیت های آهکی، آهک و یک لایه آهک شیلی تشکیل یافته و از میزان تخلخل خوب تا خیلی خوب برخوردار است. میزان ضخامت خالص در این زون متنوع بوده و از مقدار کمتر از یک متر تا ۲۱ متر (در اطراف چاه شماره ۴۳) متغیر است. مقدار ضخامت خالص در قسمت های مرکزی تاقدیس نسبت به یالها و دماغه های تاقدیس بیشتر است. مقدار ضخامت خالص به ناخالص نیز مقادیر متنوعی بوده و در قسمت های مرکزی تاقدیس خصوصاً اطراف چاههای ۱۲،۲۹،۲۸،۳۴،۴۳ از ۵/۰ بیشتر است. این نسبت در اطراف چاه شماره ۳۴ حداکثر مقدار خود (۹۸/۰) را دارا می باشد. متوسط اشباع آب ضخامت های خالص بین ۳۰ تا ۵۰ درصد بوده و در هیچ کدام از چاهها از ۳۰ درصد کمتر نیست. مقدار ستون مفید هیدروکربن در این زون به حداکثر ۶/۲ متر (چاه ۴۳) می رسد. این زون در پاره ای از چاهها کلاً آبزده می باشد (مانند چاه ۴۶ هر چند که در قسمت های میانی تاقدیس قرار دارد). مسلماً مقدار ضخامت خالص در چاههایی که خارج از بستگی افقی حفر شده اند مانند چاه ۲۷، صفر و یا ناچیز خواهد بود.
زون ۲- این لایه عمدتاً از ماسه ها ی شیلی، ماسه سنگ و ماسه های آهکی تشکیل یافته و از توسعه تخلخل خوب و خیلی خوب بعضاً متوسط برخوردار و هیدروکربن دار می باشد. بر طبق ارزیابی های به عمل آمده، این زون از کیفیت مخزن به مراتب بهتری نسبت به سایر زونها برخوردار می باشد. میزان ضخامت خالص و نسبت ضخامت خالص به کل و همچنین ستون مفید هیدروکربن در این زون بالا بوده به طوری که میزان ضخامت خالص در پاره ای از چاهها به مقدار بیش از ۳۰ متر و ستون هیدروکربن ۸ متر بالغ می شود. اصولاً زونهای ۲، ۳، ۴ و ۵ در میدان منصوری عمدتاً از ماسه سنگ تشکیل شده و با توجه به سیمان شدگی کم این ماسه سنگها، کیفیت مخزنی این افق ها بسیار بالاست. شکل ۱ صحت این مطالب را برای چاه شماره ۴۶ خاطرنشان می کند. همچنین نمودارهای موجود در شکل ۳ تغییرات میدانی پنج پارامتر پتروفیزیکی را در زون مخزنی ۲ نشان می دهند.
زون ۳- این لایه عمدتاً ار ماسه سنگ، ماسه های شیلی و آهک های دولومیتی تشکیل یافته و دارای تناوبی از توسعه تخلخل خیلی خوب تا پایین برخوردار است و در بخش میانی بصورت رگه های ضخیم هیدروکربن دار می باشد. قسمت عمده این زون ماسه سنگی بوده که در افزایش کیفیت مخزن نقش مهمی را ایفا نموده است. بر اساس مطالعات میدان انجام گرفته به طور کلی در این میدان مقدار نسبت ضخامت خالص به نا خالص نسبت به زون ۲ کاهش را نشان می دهد هر چند که گاه به بیش از ۶/۰ (چاه شماره ۴۲) می رسد این لایه ستون هیدروکربنی خوبی دارد به طور کلی این لایه تولیدی بوده و از کیفیت مخزنی نسبی مناسبی برخوردار است. زون ۴ تا ۸- از آنجایی که سطح تماس آب و نفت برای کل میدان در عمق ۲۲۷۲ متری زیر سطح دریا (۲۲۷۹ متر از سطح زمین) قرار دارد، لذا قسمت پایین زون ۳ و زونهای ۴،۵،۶،۷،۸ مخزن آسماری این میدان زیر سطح تماس آب و نفت واقع گردیده و میزان ضخامت خالص، ستون مفید هیدروکربن و نسبت ضخامت خالص به ناخالص در این زون ها صفر و یا بسیار ناچیز است.
نتیجه گیری
۱- مخزن آسماری به ۸ زون (لایه) تقسیم شده است که هر زون دارای لیتولوژی و اختصاصات پتروفیزیکی مربوط به خود است. زون یک عمدتا کربناته (آهکی و دولومیتی)، زونهای ۲، ۳،۴ و ۵ عمدتا ماسه سنگی (بخش ماسه سنگی اهواز)، زون ۶ مخلوطی از سنگ آهک، دولومیت، ماسه و شیل و زونهای ۷ و ۸ آهکی و شیلی است.
۲- مقایِسه زونهای مختلف مخزن در چاه شماره ۴۶ نشان می دهد که با افزایش عمق بر میِزان شیل و آهک بطور نسبی افزوده می شود ولی مقدار کوارتز بویژه در زونهای خاص (۲، ۳، ۴ و ۵) درصد عمده ای را تشکیل داده و در زون ۵ بمقدار کم یافت می شود. میزان دولومیت بطور نسبی با افزایش عمق کاهش می یابد و بیشترین مقدار آن در زون ۱ مشاهده می شود.
۳- درصد اشباعی آب و نفت در چاه شماره ۴۶ در زون ۲ و ۳ بترتیب کاهش و افزایش می یابد و این نشانه تمرکز نفتی بیشتر در بخشهای ماسه سنگی است. در زون ۱ که یک زون آهکی- دولومیتی است تغییرات این دو پارامتر قابل توجه است ولی درصد اشباع نفت آن از زونهای ۲ و ۳ کمتر می باشد.
۴- تغییرات درصد اشباع آب و نفت در مخزن حاکی از کنترل لیتولوژیکی توزیع نفت است، بطوریکه در زون ۲ و ۳ بدلیل بالا بودن درصد ماسه سنگ، بیشترین مقدار را داراست. در این زون فرایند دولومیتیزاسیون غالب نیست.
۵- بر اساس ارزیابی های به عمل آمده زون ۲ با بیش از ۸۰ درصد ماسه بیشترین ستون مفید هیدروکربنی، ضخامت خالص و نسبت ضخامت خالص به کل را دارا بوده و نظر به اشباع آب کم آن (۲۰ درصد برای زون های مفید)، بهترین کیفیت مخزنی را در بین زون های دیگر دارا می باشد. پس از آن زون های ۳ و ۱ از کیفیت مخزنی مناسب تری برخوردارند. از آنجایی که زونهای ۴ تا ۸ زیر سطح تماس آب و نفت قرار دارند، لایه تولیدی نبوده و از کیفیت مخزنی پایینی برخوردارند. زون ۲ بهترین لایه تولیدی نفت از نظر پارامترهای پتروفیزیکی به شمار می رود.
منابع
۱- مطیعی، ه. ،۱۳۷۲، زمینشناسی ایران، چینهشناسی زاگرس، سازمان زمینشناسی کشور.
۲- Durrast, H., & Siegesmund, S., 1999, Correlation between rock fabrics and physical properties of carbonate reservoir rocks, Int. J. Earth Sci., 88, 392-408. 3- Jardine, D., & Wilshart, J.W., 1987, Carbonate reservoir description. Soc. Econ. Paleont. Min., Spec. Publi., 40, 129-152 4- Lucia, F. J., 1999, Carbonate reservoir rocks, Springer-verlog Berlin Heidelberg New York, 226 P. 5- Luo, P., & Machel, H.G., 1995, Pore size and pore throat types in a heterogeneous dolostone reservoir, Devonian Grosmont Formation, Weste Canada sedimentary basin. Am. Assoc. Petr. Geol. Bull. Vol. 79, P. 1698-1720. 6- Murray, R. C.,& Pray, L.C., 1965, Dolomitization and limestone digenesis, An introduction, Soc. Econ. Paleont. Min., Spec. Publi., 13, 1-2 7- Nelson, R. A., 1985, Geological analysis of naturally fractured reservoirs. Gulf Publishing, Houston, pp.1-320 8- Schlumberger, 1989, Log interpretation/ Application, 2 nd edition, Schlumberger Well Services. 9- Sun, S.Q., 1995, Dolomite reservoirs: Porosity evolution and reservoir characterization, AAPG Bull., 79, 186-204 10- Wardlaw, N.C., 1965, Pore geometry of carbonate rocks, as revealed by pore casts and capillary pressure, AAPG Bull., 60, 245-257. 11- Warren, J., 2000, Dolomite: occurrence, evolution and economically important associations, Earth Science Reviews Vol. 52, P. 1-81 12- Zenger, D.H., Dunham, J.B., & Ethington, R.L., 1980, Concepts and models of dolomitization, Soc. Econ. Paleont. Min., Spec. Publi., 28, 1-320.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 298 تاريخ : يکشنبه 21 تير 1388 ساعت: 14:2
یک بخش از شیمی فضایی ، ایزومری فضایی است. ایزومرها ترکیبات متفاوتی هستند که فرمول مولکولی یکسانی دارند. ایزومرهای خاصی که فقط از نظر جهت گیری اتمها در فضا باهم تفاوت دارند اما از نظر نحوه اتصال اتمها به یکدیگر ، شبیه یکدیگرند، ایزومرهای فضایی نام دارند.
یک بخش از شیمی فضایی ، ایزومری فضایی است. ایزومرها ترکیبات متفاوتی هستند که فرمول مولکولی یکسانی دارند. ایزومرهای خاصی که فقط از نظر جهت گیری اتمها در فضا باهم تفاوت دارند اما از نظر نحوه اتصال اتمها به یکدیگر ، شبیه یکدیگرند، ایزومرهای فضایی نام دارند.
شباهت و تفاوت ایزومرهای فضایی
تفاوت جفت ایزومرهای فضایی از نظر ساختار و بنابراین از نظر خواص بسیار کوچک است. اما از نظر همه خواص فیزیکی قابل سنجش ، با یکدیگر مشابهند مگر از نظر تاثیر بر نوعی نور غیر عادی. با استفاده از همین تاثیر متفاوت و دستگاه خاص مربوطه میتوان دو ایزومر را از یکدیگر باز شناخت.
کاربرد متفاوت ایزومرهای فضایی
با وجود شباهت نزدیک ، وجود اینگونه ایزومرها ، یکی از سنجشگرهای بسیار حساس را برای تشخیص مکانیسم واکنشها در اختیار شیمیدان میگذارد. غالبا یکی از این ایزومرها برای مطالعه برگزیده میشود. نه به این دلیل که این ایزومرها از نظر شیمی سه بعدیاش با ترکیبهای دیگر فرق دارد، بلکه به این دلیل که این ترکیب میتواند نکتههایی را آشکار سازد که در ترکیبهای عادی پنهاناند و باز هم با وجود شباهت نزدیک دو ایزومر فضایی ، ممکن است یکی از آنها یک غذای مقوی یا یک آنتی بیوتیک یا یک داروی محرک قلب باشد، ولی ایزومر دیگر ترکیبی بیمصرف باشد.
تعداد ایزورمها و کربن چهار وجهی
باید در نظر داشت که هر ترکیبی ولو پیچیده که دارای کربنی متصل به چهار اتم دیگر است را میتوان مشتقی از متان تلقی کرد و آنچه که درباره شکل مولکول متان فرا میگیریم را میتوانیم درباره شکل مولکولهای پیچیده بکار بریم. برای هر اتم ، فقط یک ماده با فرمول یافت شده است. با کلردار کردن متان ، فقط یک ترکیب با فرمول و با برمدار کردن آن فقط یک ترکیب با فرمول بدست میآید. به همین ترتیب فقط یک و یک شناخته شده است.
در واقع ، اگر ، بجای اتم نمایاننده یک گروه از اتمها باشد نیز مطلب فوق صادق است، مگر هنگامی که گروه تا آن حد پیچیده است که خود سبب ایزومری میشود. به عنوان مثال فقط یک ، یک و یک وجود دارد. این نشان میدهد که در متان ، همه اتمهای هیدروژن هم ارزند، بطوری که با جایگزین کردن هر کدام از آنها ، فرآورده یکسانی حاصل میشود. اگر اتمهای هیدروژن متان هم ارز نبودند، با جایگزین کردن هر کدام از آنها ترکیب متفاوتی بدست میآمد و فرآوردههای استخلافی ایزومری حاصل میشدند.
برای اتمهای هیدروژن در متان سه آرایش امکان پذیر است که هم ارز باشند:
آرایش مسطح که در آن اتم کربن در مرکز یک مستطیل یا مربع و اتمهای هیدروژن در چهار گوشه آن قرار دارند.
آرایش هرمی که در آن اتم کربن در راس هرم و اتمهای هیدروژن در چهار گوشه آن قرار دارند.
آرایش چهار وجهی که در آن کربن در مرکز چهار وجهی و هر اتم هیدروژن در یک گوشه آن است.
فعالیت نوری
نور خواصی دارد که با در نظر گرفتن آن به عنوان یک پدیده موجی بخوبی درک میشوند. موجی که در آن ارتعاشها بصورت عمود بر جهت حرکت نور روی میدهند. تعداد سطحهایی که از خط مسیر نور میگذرند بیشمارند و نور معمولی در همه این سطوح در حال ارتعاش است. اگر مستقیما به باریکهای از نور یک لامپ بنگریم، نوع ارتعاشهایی که روی میدهند و همگی عمود بر خط بین چشمان ما و منبع نور (لامپ) هستند را نشان میدهد.
نور معمولی ، با عبور کردن از یک عدسی ساخته شده از مادهای به نام "پلاروید" یا از یک قطعه کلسیت (نوعی بلور ) با آرایشی که به نام منشور نیکول معروف است، به نور قطبیده در سطح تبدیل میشود. یک ماده فعال نوری ، مادهای است که سطح نور قطبیده را میچرخاند. وقتی نور قطبیده در حال ارتعاش در یک سطح معین ، از میان یک ماده فعال نوری میگذرد، در حال ارتعاش در یک سطح دیگر پدیدار میشود.
پلاریمتر
چگونه میتوان این چرخش سطح نور قطبیده یعنی این فعالیت نوری را تشخیص داد؟ این پدیده را با استفاده از دستگاهی به نام پلاریتمر میتوانیم تشخیص دهیم و اندازه گیری کنیم. ما نه تنها میتوانیم چرخیدن سطح و نیز جهت آن را تشخیص دهیم، بلکه مقدار این چرخش را هم میتوانیم تعیین کنیم.
چرخش ویژه
از آنجا که چرخش نوری مورد توجه ما از مولکولهای مجزای ترکیبهای فعال ناشی میشود، مقدار چرخش به تعداد مولکولهای موجود در لوله که نور به آنها برخورد میکند، بستگی دارد. در مقایسه با یک لوله 10 سانتیمتری ، در لوله 20 سانتیمتری امکان برخورد نور با مولکولها دو برابر است و در نتیجه چرخش نیز دو برابر است. اگر ترکیب فعال بصورت محلول باشد، تعداد مولکولهای برخورد کننده با نور ، به غلظت محلول بستگی خواهد داشت.
در لولهای بطور ثابت ، در مقایسه با محلولی با غلظت یک گرم در 100ml حلال ، در غلظت دو گرم در 100ml ، تعداد برخورد بین مولکولها و نور دو برابر است و در نتیجه مقدار چرخش نیز دو برابر است. با روشن شدن اثر طول لوله و غلظت بر چرخش ، معلوم می شود که مقدار چرخش و نیز جهت آن ، یک خصلت مشخصه هر ترکیب فعال نوری است. چرخش ویژه یعنی تعداد درجههای چرخش مشاهده شده در صورتی که لولهای بطول یک دسیمتر ، 10 سانتیمتر مورد استفاده قرار گیرد و غلظت نمونه 1 باشد.
معمولا این چرخش ، با استفاده از لولههایی با طولهای مختلف و غلظتهای متفاوت از رابطه زیر محاسبه میشود.
(X = α/(1Xd
(gr/ml) طول (dm)/چرخش مشاهده شده (درجه) = چرخش ویژه
در این رابطه ، d نمایاننده چگالی یک مایع خالص یا غلظت یک محلول است.
چرخش ویژه نیز همانند دمای ذوب ، دمای جوش ، چگالی ، ضریب شکست و... یکی از خواص یک ترکیب است. به عنوان مثال ، چرخش ویژه 2- متیل -1- بوتانول بدست آمده از روغن فوزل چنین است.
انانتیومر
ایزومرهایی که تصویر آینهای یکدیگرند را انانتیومر می گویند. دو اسید لاکتیک متفاوتی که مدلهای فضایی متفاوتی دارند و ایزومر فضایی هستند، انانتیومر هستند (در زبان یونانی: enantio به معنای مخالف). دو ، 2- متیل -1- بوتانول ، دو ، Sec - بوتیل کلرید و غیره نیز انانتیومر هستند. انانتیومرها خواص فیزکی مشابهی دارند، مگر از نظر جهت چرخاندن سطح نور قطبیده.
به عنوان مثال ، دو ، 2- متیل -1- بوتانول دارای دمای ذوب ، دمای جوش ، چگالی ، ضریب شکست و خواص فیزیکی دیگر یکسانند و تنها تفاوت آنها این است که نور قطبیده در سطح را یکی به راست و دیگری به چپ می چرخاند. این واقعیت تعجب برانگیز نیست. چون برهمکنشهای دو نوع مولکول با دوستانشان باید یکسان باشد. فقط جهت چرخش متفاوت است. مقدار چرخش یکی است. انانتیومرها خواص مشابهی دارند مگر از نظر واکنش با واکنشگرهای فعال نوری.
کایرالیته
مولکولهایی که بر تصویر آیینهای خود قابل انطباق نیستند، کایرال هستند. کایرالیته ، شرط لازم و کافی برای موجودیت انانتیومرهاست. مثل این است که بگوییم: ترکیبی که مولکولهایش کایرال هستند، میتوانند بصورت انانتیومرها وجود داشته باشند. ترکیبی که مولکولهایش ناکایرال هستند (فاقد کایرالیته) ، نمیتوانند بصورت انانتیومرها وجود داشته باشند.
مخلوط راسمیک
مخلوطی از انانتیومرها به مقدار مساوی را مخلوط راسمیک میگویند. یک مخلوط راسمیک از نظر نوری غیرفعال است. هنگامی که دو انانتیومر باهم مخلوط میشوند، چرخش ایجاد شده توسط یک مولکول ، دقیقا با چرخش مخالف ایجاد شده توسط مولکول انانتیومر خود خنثی میشود. پیشوند برای مشخص کردن ماهیت راسمیک یک نمونه خاص بکار میرود، مانند (±) - لاکتیک اسید یا ± -2- متیل -1- بوتانول.
خوب است مخلوط راسمیک را با ترکیبی مقایسه کنیم که مولکولهایش به تصویر آینهای خود قابل انطباق هستند. یعنی ترکیب ناکایرال. هر دو ، دقیقا به دلیل یکسانی غیر فعال نوری هستند. به علت توزیع تصادفی تعداد زیادی مولکول ، به ازای هر مولکولی که با نور برخورد میکند، مولکول دومی وجود دارد که تصویر آیینهای آن است و دقیقا طوری جهت گیری کرده است که اثر مولکول اول خنثی کند. در یک مخلوط راسمیک ، مولکول دوم ایزومر مولکول اول ایزومر مولکول اول است. در یک ترکیب ناکایرال ، مولکول دوم ایزومر مولکول اول نیست، بلکه مولکول دیگری همانند مولکول اول است.
سایت رشته صنایع شیمیایی...
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 276 تاريخ : شنبه 20 تير 1388 ساعت: 17:56
کتاب شیمی نو (سال دوم دبیرستان) سال 1340 هجری شمسی (کتاب شیمی 47 سال پیش!)
کتاب شيمی نو در سال 1340 توسط آقايان قلی زاده، امين، حاج سيد جوادی، نوروزيان، اردلان، رفيع زاده، رهنما، صفری و بروخيم در 70 صفحه برای سال دوم دبیرستان به رشته تحرير درآمده است.

این کتاب مبتنی بر آزمایش و در 70 صفحه نوشته شده است و شامل مباحثی مانند اثر اسيدها بر چند فلز، تبخير و نشان دادن نمک های محلول در آب و شناختن بعضی از اجسام شيميايی به وسيله يکديگر و ... می باشد. در آخر هر فصل نيز تعدادی تمرين ارائه گرديده است. هم چنین در انتهای کتاب مفاهیمی مانند عنصر و اتم و جرم اتمی و ترکیب و ... توضیح داده شده است.
توصیه می کنیم این کتاب جالب را دانلود کنید و کتاب 47 سال پیش را با کتاب های شیمی امروز مقایسه کنید.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 235 تاريخ : شنبه 20 تير 1388 ساعت: 8:34
پس از عملیات حفر چاه و اصابت آن به مخزن نفت، به دلیل فشار زیاد موجود در مخزن، جریان نفت به سوی دهانه خروجی چاه سرازیر می شود. این مرحله از استخراج که عامل آن فشار داخل خود مخزن است به بازیافت اولیه نفت موسوم است. در برداشت اولیه نفت ، از انرژی خود مخزن برای تولید نفت استفاده می شود.البته این بدان معنا نیست که اگر نفت خود به خود به سطح زمین نیاید، برداشت اولیه وجود نخواهد داشت،بلکه وقتی از پمپ برای بالا آوردن نفت استفاده میکنیم،در واقع هنوز در مرحله اول برداشت نفـــــــت قرار داریم.در این مرحله انرژی خاصی وارد مخزن نمی شود.با افزایش تولید و کاهش فشار، سرعت تولید نیز کاهش می یابد تا اینکه فشار به حدی میرسد که دیگر نفت خارج نمی شود. در این مرحله ممکن است ار ۳۰ تا ۵۰ درصد کل نفت مخزن استخراج شود. علاوه بر فشار مخزن عوامل دیگری منند خواص سنگ مخزن و میزان تخلخل آنها و همچنین دمای مخازن نیز در میزان تولید مؤثرند.
به عنوان مثال، کل نفت مخازن آمریکا حدود۱۰۹*۴۰۰ بشکه بوده است که تا سال ۱۹۷۰ حدود ۱۰۹*۱۰۰ بشکه آن توسط روشهای اولیه استخراج شده اند.البته هر چه میزان گاز آزاد در مخزن بیشتر باشد مقدار تولید نفت توسط این روش بیشتر است، زیرا تغییرات حجم گاز در مقابل تغییر فشار بسیار زیاد است. به عنوان مثال در ایالت پنسیلوانیای آمریکا به دلیل پایین بودن نفوذپذیری (کمتر از ۵۰ میلی دارسی) و انرژی کم مخزن که ناشی از پایین بودن مقدار گاز طبیعی آزاد است، میزان نفت استخراج شده با روشهای اولیه بین ۵ تا ۲۵ درصد کل نفت بوده است و به همین دلیل در این ایالت روشهای مرحله دوم از سال ۱۹۰۰ شروع شده است.
وقتی مخزن تخلیه شد و ما نتوانستیم نفت را حتی با پمپاژ از مخزن به چاه و از چاه به سطح زمین انتقال دهیم،در این صورت استفاده از روش EOR از نوع بازیافت ثانویه شروع میشود که برای استفاده از این روش، امروزه در دنیا روش تزریق آب مرسوم است. در این روش از چاه تزریقی،آب به مخزن تزریق میشود و از چاه بهره برداری،نفت مورد بهره برداری قرار می گیرد.در این روش،ما با تزریق سیال در سیستم مداخله میکنیم و سیال تزریقی،نفت را به طرف چاه تولیدی هدایت میکند. البته به جای آب،میتوان گاز نیز تزریق کرد که به آن فرایند تزریق گاز می گویند. باید توجه داشت که استفاده از این دو روش تزریقی با تزریق آب یا گازی که به منظور حفظ و نگهداری فشار مخزن انجام میگیرد متفاوت است. چرا که در تزریق آب و گاز برای حفظ فشار مخزن، سیال تزریقی باعث حرکت نفت نمی شود،بلکه از افت سریع فشار مخزن در اثر بهره برداری جلوگیری می کند.
در حالت ثانویه برداشت زمانی فرا میرسد که، ما ضمن تزریق آب به مخزن،در چاه تولیدی با تولید آب مواجه می شویم. در این حالت، چون نسبت آب به نفت زیاد میشود و تولید در این صورت بازده اقتصادی ندارد،باید از روش دیگر برای افزایش برداشت بهره بگیریم.اگر تزریق آب را متوقف کنیم و از فرایند های دیگری نظیر تزریق گاز CO2 استفاده کنیم. از روشهای مؤثر در مرحله دوم یکی سیلابزنی آبی و دیگری سیلابزنی گازی یا تزریق گاز است.
در روش سیلابزنی آبی، آب با فشار زیاد در چاههای اطراف چاه تولید نفت وارد مخزن شده و نیروی محرکه لازم رای استخراج نفت را به وجود می آورد.معمولا در اطراف هر چاه نفت چهار چاه برای تزریق آب وجود دارد. در روش سیلابزنی گازی، گاز (مانند گاز طبیعی ) با فشار زیاد به جای آب وارد مخزن شده و نفت را به طرف چاه خروجی به جریان می اندازد. در کشور ونزوئلا حدود ۵۰% گاز طبیعی تولید شده دوباره به چاههای نفت برای استخراج در مرحله دوم برگردانده می شود. نحوه تزریق گاز شبیه تزریق آب به صورت چاههای پنجگانه است. در مواردی که گرانروی نفت خیلی بالا باشد از تزریق بخار آب برای استخراج مرحله دوم استفاده میشود. تزریق بخار آب، دما را افزایش و گرانروی را کاهش میدهد. در این روش که از بخار آب به جای آب استفاده میشود، با کاهش گرانروی نفت، جریان آن راحت تر صورت گرفته و سرعت تولید بالا می رود.
پس از استخراج به کمک روشهای مرحله دوم هنوز هم حدود ۳۰ الی ۵۰ درصد نفت میتواند به صورت اسنخراج نشده در مخزن باقی بماند. در اینجاست که استخراج نفت به کمک روش مرحله سوم صورت گیرد. یکی از روشهای مرحله سوم، تزریق محلول مایسلار (micellar solution) است که پس از تزریق آن، محلولهای پلیمری به عنوان محلولهای بافر به چاه تزریق می شود. در آمریکا ممکن است روشهای استفاده از محلولهای مایسلار تا ۵۰ درصد کل روشهای مرحله سوم را شامل شود. محلول مایسلار مخلوطی از آب، مواد فعال سطحی، نفت و نمک است. در روشهای جدید تهیه محلول مایسلار ، نفت، نمک و مواد کمکی فعال سطحی حذف گردیده اند. محلولهای مایسلار نیروی تنش سطحی بین آب و نفت را تا حدود dyne/cm 001/0 یا کمتر از آن کاهش میدهد.
گرانروی محلول پلیمری حدود ۲ تا ۵ برابر گرانروی نفـــــــــــت است. غلظت پلیمر حدود ppm1000 می باشد. در حال حاضر از پلی اکریمید ها و زیست پلیمر ها به عنوان پلیمر در محلول بافر استفاده می شود. مواد فعال سطحی معمولا سولفوناتهای نفتی سدیم هستند و از لحاظ خواص و ساختار شیمیایی شبیه شوینده ها می باشند. از الکلها برای مواد کمکی فعال سطحی استفاده می شود.هزینه تهیه محلولهای مایسلار برای تولید هر بشکه نفت در سال ۱۹۷۵ حدود ۵/۱ دلار آمریکا بوده است.
یکی دیگر از روشهای مرحله سوم، روش احتراق زیر زمینی است. طی این روش اکسیژن موجود در هوا در زیر زمین با هیدروکربنها می سوزد و مقداری انری و گاز تولید شده، فشار مخزن بالا میرود.گرما همچنین گرانروی را کاهش داده و جریان نفت راحتتر صورت میگیرد. یک روش دیگر مرحله سوم که اخیرا مورد توجه قرار گرفته است، روش تزریق گاز کربن دی اکسید می باشد که جزئی از روش جابجایی امتزاج پذیر است. گاز کربن دی اکسید بسیار ارزان بوده، در نفت نیز حل میشودو گرانروی ان را کاهش می دهد.از روشهای دیگر مررحله سوم انفجار های هسته ای در زیر زمین است که این انفجار ها شکاف مصنوعی در سنگها به وجود می آورد و جریان نفت را ساده تر میکند. به این گونه فراینـــــد ها، مرحله سوم برداشت نفــت (Tertiary Oil Recovery) می گویند.
گفتنی است که مراحل برداشت نفت را به گونه ای دیگر میتوان تقسیم بندی کرد، یعنی به جای اینکه بگوئیم مرحله اول،دوم یا سوم، می توانیم بگوییم Primary Recovery ، مرحـله Improved Oil Recovery یا IOR و مرحله EOR یا Enhanced Oil Recovery.
برداشت بهبود یافته یا IOR فرایندی است که برای تعدیل کردن تکنولوژی های مورد استفاده برای افزایش برداشت بکار میرود. حال این فرایند می تواند در مرحله اول تولید انجام شود یا در مراحل دوم و سوم. تکنولوژی هایی چون حفاری افقی یا مشبک کاری انتخابی و یا تزریق ژل در جا (Insitu gelation) از نوع IOR میباشند.
بنابراین در IOR فرایند تولیـد عوض نمیشود، بلکه تکنولوژی به گونه ای تعدیل می شود که با همان فرایند قبلی،نفت بیشتری از مخزن تولید می گردد. در حالی که ازدیاد برداشت یا EOR به فرایندی اطلاق می شود که در آن سعی میشود تا میزان درصد اشباع نفت باقیمانده تا آنجا که ممکن است پایین بیاید و نفت باقیمانده در مخزن به حداقل ممکن برسد. فرایند هایی چون سیلابزنی شیمیایی، تزریق CO2 و احتراق درجا از این قبیل میباشند. بعد از عملیات تزریق آب میتوان فرایند را تغییر داد. روش دیگری این است که عملیات تزریق آب را تعدیل کنیم. بدین منظور در لایه های با خاصیت گذر دهی متفاوت، آب وارد لایه های با خاصیت گذردهی بالا شده و به سمت چاه تولیدی هدایت میگردد، لذا باید کاری کرد که این لایه ها بسته شوند. این کار با تزریق ژل در لایه های مورد نظر صورت می گیرد.فرایند جابه جایی امتزاجی (Miscible Displacement) به معنی بازیافت نفت به وسیله تزریق ماده ای است که با نفت قابل امتزاج باشد. در جابه جایی مذکور سطح تماس نفت و ماده تزریق شده از بین می رود و جابه جایی بصورت حرکت تک فازی انجام میشود. در صورتی که شرایط از هر لحاظ برای امتزاج ماده تزریق شده و نفت فراهم باشدبازیافت چنین فرایندی در مناطق جاروب شده ۱۰۰% میباشد.
گاز تزریقی دارای ویسکوزیته کمتر نسبت به نفت مخزن است و در نتیجه تحرک بیشتری نسبت به آن دارد.این خاصیت گاز تزریقی،یکی از دلایل امکان امتزاج آن با نفت مخزن است، زیرا تحرک زیاد گاز نسبت به نفت باعث می شود که گاز در مراحل مختلفی با نفت تماس پیدا کرده و در نهایت حالت امتـزاج بین نفت مخزن و گاز تزریقی حاصل آید.
مسئله ای که از تحرک زیــاد گاز ناشی می شود این است که گاز تمایل به Fingering و Channeling پیدا میکند و در نتیجه مناطقی از مخزن به وسیله گاز جاروب نمی گردد و لذا این امر باعث پایین آمدن Recovery Factor در جابه جایی امتزاجی میشود.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 251 تاريخ : شنبه 20 تير 1388 ساعت: 8:31
وابسپارش گرمایی رویهای برای تبدیل مواد آلی پیچیده به نفت خام سبک است. این رویه تقلیدی از جریان طبیعی زمینشناختی است که در ساخت سوخت فسیلی اتفاق میافتد. در فشار و گرمای زیاد زنجیرههای بلند بسپار هیدروژن، اکسیژن، و کربن متلاشی شده و به شکل زنجیرههای کوتاه ترکیبات هیدروکربن با بیشینهٔ ۱۸ کربن درمیآیند.
از فوریه ۲۰۰۵ کارخانهای آزمایشی در ایالت میسوری امریکا با استفاده از زائدات بوقلمون روزانه ۴۰۰ بشکه نفت خام سبک تولید میکند. هزینهٔ تمام شده ۸۰ دلار برای هر بشکه گزارش شده است. این هزینه برای موادی که دارای کربن بیشتری باشند، مانند بطریهای پلاستیکی، کمتر خواهد بود.
نفت مایعی غلیظ و افروختنی به رنگ قهوهای سیر یا سبز تیره است که در لایههای بالایی بخشهایی از پوسته کره زمین یافت میشود. نفت شامل آمیزه پیچیدهای از هیدروکربنهایی گوناگون است. بیشتر این هیدروکربنها از زنجیره آلکان هستند ولی ممکن است از دید ظاهر، ترکیب یا خلوص تفاوتهای زیادی داشته باشند. ریشه واژه نفت از واژه اوستایی «نافتا» است. در برخی منابع قدیمی به صورت نفط نیز آمده است. نفت از باقی مانده حیوانات وگیاهانی که میلیونها سال قبل از محیط دریا (آب)،قبل از دایناسور ها زندگی می کردند ،تشکیل شده است .در طی سالها ،باقی مانده ها توسط لپه های گل پوشیده شده است .گرما وفشار این لپه ها به این باقی مانده ها کمک کرد تا به چیزی تبدیل شوند که ما امروزه نفت خام می دانیم . نفت ها از کجا آمده است؟ نفت خام ،یک مایع زرد تا سیاه ،بودار می باشد ،معمولا در نواحی زیر زمینی که مخازن نامیده می شود ،یافت می شود .دانشمندان و مهندسان یک منطقه انتخاب شده تا مطالعه نمونه های سنگی زمین را مورد استخراج قرار می دهد .اندازه گیریها انجام می شود واگر مکان از لحاظ نفتی مکان موفقیت آمیزی باشد ،حفاری آغاز می شود .بالای چاه ساختاری که (گل)نامیده می شود ،برای جا دادن وسایل ولوله ها ی مورد استفاده در چاه ساخته می شود .زمانی که حفاری تمام می شود ،چاه حفر شده یک جریان ثابتی از نفت را به سطح زمین خواهد آورد .
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 238 تاريخ : شنبه 20 تير 1388 ساعت: 8:30
تخمیر پدیدهای است ناشی از مجموعه فعالیتهای زیستی که در آن ترکیبات آلی دارای مولکولهای بزرگ به ترکیبات دارای مولکولهای کوچکتر و سادهتر شکسته و تجزیه (کاتابولیسم) شده از فرآیند آن علاوه بر ایجاد ترکیبات آلی سادهتر، دیاکسیدکربن و انرژی نیز آزاد میگردد. با بیان دیگر تخمیر تجزیه ناقص بعضی از متابولیتها (ترکیبات آلی) به ترکیبات سادهتر همراه با انرژی توسط عامل تخمیری است.
در گیاهان تخمیر بیولوژیکی تنها تخمیر الکلی نبوده، ممکن است با کمی تخمیر لاکتیک نیز همراه باشد، برخی از سازوارههای حیاتی (میکروارگانیسمها) مانند قارچهای میکروسکوپی نیز قادر به تخمیرهایی مانند تخمیرهای سیتریک و اکسالیک روی قندهای شش کربنی (هگزوزها) و تخمیر استیک روی الکل اتیلیک و غیره هستند. باکتریها عامل انواع دیگری از تخمیر در طبیعت هستند. تخمیر بوتیریک سلولز لاشه برگها و تجزیه آنها که سبب افزایش ترکیبات آلی خاک میشود و همچنین تخمیرهای تعفنی مواد آلی توسط باکتریها صورت میگیرد.
در گیاهان تخمیر بیولوژیکی تنها تخمیر الکلی نبوده ، ممکن است با کمی تخمیر لاکتیک نیز همراه باشد، برخی از سازوارههای حیاتی (میکروارگانیسم|میکروارگانیسمها) مانند قارچهای میکروسکوپی نیز قادر به تخمیرهایی مانند تخمیرهای سیتریک و اکسالیک روی قندهای شش کربنی (هگزوزها) و تخمیر استیک روی الکل اتیلیک و غیره هستند. باکتریها عامل انواع دیگری از تخمیر در طبیعت هستند. تخمیر بوتیریک سلولز لاشه برگها و تجزیه آنها که سبب افزایش ترکیبات آلی خاک میشود و همچنین تخمیرهای تعفنی مواد آلی توسط باکتریها صورت میگیرد.
تخمیر الکلی
مخمر الکلی
پاستور اولین کسی است که نقش مخمرهای الکلی را نشان داد. بهترین مثال مخمرها ، مخمرهای خمیرترش یا مخمر نانوایی است. اگر این مخمرها در محیط کشت گلوکز و در حضور اکسیژن کافی قرار گیرند، به شدت تقسیم شده ، اکسیژن جذب کرده ، دیاکسیدکربن آزاد میسازند. بیشترین سرعت واکنشهای ناشی از تنفس و شدت اکسیداسیون گلوکز این مخمرها که از گروه آسکومیست هستند هنگامی است که تنفس هوازی دارند اگر این مخمرها در داخل یک ظرف در بسته کشت داده شوند پس از مصرف اکسیژن محدود و معین داخل ظرف و آزاد ساختن گازکربنیک دیگر قادر به تنفس عادی نبوده ، شروع به تخمیر باقی مانده مواد میکنند. آغاز تخمیر ایجاد اکسیدکربن همراه با الکل اتیلیک است و بوی الکل اتیلیک در این هنگام وقوع عمل تخمیر را در محیط کشت معلوم میکند.
تخمیر همیشه با تشکیل الکل همراه نیست، در تخمیر ترکیبات دیگری مانند گلیسیرول نیز بوجود میآیند. پیدایش ترکیبات فرعی غیر از الکل در پدیده تخمیر و حضور این ترکیبات در محیط عمل از نظر ادامه تغییر اهمیت فراوان دارد. رشد مخمرها در شرایط تخمیری (تنفس بیهوازی) بسیار کند است، در شرایط تخمیر انرژی آزاد شده از مقدار معینی مواد قندی مانند یک گرم گلوکز محلول ، درحدود 21 بار کمتر از حالت تنفس عادی (هوازی است) انرژی حاصل از پدیده تخمیر بیشتر به صورت حرارت تلف میشود.
محیط در حال تخمیر نسبت به محیطی که در آن تنفس عادی صورت میگیرد بسیار گرمتر است. تخمیر الکلی تحت اثر مجموعه در همی از آنزیمهای درون سلولی به نام (زیماز) صورت میگیرد. مجموعه آنزیمی هنگامی که مخمرهای آن زنده باشند بیشترین اثر تخمیری را دارند. بازده تخمیری آنزیمها در خارج از سلول بسیار ضعیفتر از آنزیمهای داخل سلول زنده است. بین اثر طبیعی آنزیمها ، نیروی زیستی و ساختار سلولی مخمرها بستگیهایی وجود دارد و به اصطلاح تخمیر پدیدهای درون سلولی است و آنزیمهای استخراج شده از مخمرها در خارج از سلول بخش مهمی از قدرت تخمیری خود را از دست میدهند.
تخمیر واقعی یا حقیقی
هنگامی در ذخایر قندی یک بافت پیش میآید که در شرایط عادی از هوا قرار داشته ، در آن تنفس بی هوازی پیش آید. اگر بخشی از یک بافت ذخیرهای دارای مواد قندی ، مانند قطعاتی از غده چغندر بخش از میان بر میوههای آبدار و شیرین مثل انگور را داخل یک ظرف در بسته با مانومتر قرار دهیم، در بافتهای قطعات مزبور ابتدا تنفس عادی با جذب اکسیژن و دفع دیاکسیدکربن صورت میگیرد. از آنجا که اکسیدکربن حاصل از تنفس عادی بعدا در داخل شیره واکوئلی سلولهای بافت حل میشود، فشار داخلی ظرف با جذب اکسیژن موجود به تدریج کم میشود وقتی اکسیژن درون ظرف تمام شده به ناچار شرایط بیهوازی (تخمیر) پیش آمده ، با ازدیاد تدریجی اکسیدکربن و الکل در ظرف ، بالا رفتن فشار داخلی آن شروع میشود.
تخمیر بوسیله خود بافتها و بدون حضور میکروارگانیسمها و مخمرها صورت گرفت. این تخمیر که در کلیه بافتهای گیاهی ، میوههای سبز مانده در تاریکی و حتی در جلبکها و قارچها نیز کم و بیش دیده میشود تخمیر درون بافتی و عاری از مخمر میگویند. تخمیر درون بافتی در بسیاری از دانههای جوان مانند نخود که پوسته آن نسبت به اکسیژن تا اندازهای قابل نفوذ است و همچنین در بیشتر میوههای آبدار که اکسیژن در بافتهای داخلی آنها معمولا کم است امری عمومی است.
به خصوص اگر مقدار زیادی میوه در یک جا انبار شود، موجبات و شرایط تخمیر در آنها کاملا فراهم میشود. با توجه به مطالب فوق و تخمیر درون بافتی ، باید آن را پدیدهای عمومی در گیاهان دانست و توجه به این امر که آنزیمهای تشکیل دهنده زیماز منشا گیاهی دارند، تخمیر را باید امری طبیعی در گیاهان به شمار آورد. پدیده تخمر درون بافتی با مرگ سلولهای بافت مورد تخمیر معمولا ارتباط ندارد، اگر بافتهای در حال تخمیر در هوای آزاد قرار داده شوند، تخمیر درونی آنها متوقف شده تنفس عادی مجددا آغاز میشود. تخمیر در گیاهان فقط از نوع الکلی نیست همراه با ایجاد الکل ترکیبات دیگری مانند اسید سیتریک ، اسید مالیک ، اسید اکسالیک و اسید تارتاریک نیز کم و بیش بوجود میآیند.
شدت تخمیر و اندازه گیری آن
شدت تخمیر را با قرار دادن اندام دارای ذخیره قندی مانند دانهها ، غدهها و یا میوهها در یک محیط فاقد اکسیژن و دارای ازت میتوان به دقت اندازه گرفت و برای این سنجش از روش اندازه گیری دیاکسیدکربن آزاد شده نیز میتوان استفاده کرد. ولی چون واکنشهای دیگر همزمان با تخمیر میتوانند CO2 متصاعد کنند این روش ممکن است دقیق نباشد. بنابراین اندازه گیری مقدار الکل تولید شده از تخمیر معمولا بهتر میتواند معرف و تعیین کننده شدت تخمیر باشد. مقدار الکل حاصل از تخمیر در واحد زمان در یک ترکیب قندی تقریبا معادل همان نسبتی است که از اندازه گیری شدت تنفس به دست میآید.
مکانیسم تخمیر
مکانیسم تخمیر الکلی تقریبا مشابه مکانیسم تنفس عادی است و در بیشتر پیامدهای واکنشی ، همانند هم هستند. برای مطالعه مکانیسم تخمیر ، به واکنشهای تخمیر الکلی میپردازیم. تخمیر الکلی فقط روی گلوسیدها صورت گرفته ، خود شامل دو مرحله است:
مرحبه اول
انتهای پیامدهای واکنشی که حالت زنجیرهای دارند، همان مسیر EMP یا گلیکولیز است که به تشکیل اسید پیروویک ختم میشود.
مرحله دوم
با تجزیه اسید پیروویک که خود سرآغاز پیامدهای واکنشی جداگانهای است که به هیچ وجه ادامه یا بخشی از مسیر گلیکولیز نیست شروع میشود. اسید پیروویک با آنکه در آخر مسیر گلیکولیز و پایان تمام پیامدهای زنجیرهای آن مانند هگزوزها ، تری اوزها و همه اوزهای شکسته و تخریب یافته قرار دارد خود از گلوسیدها به شمار نمیآید. شروع تخمیر الکلی از راه گلیکولیز با استالوئید است. استالوئید را میتوان بوسیله سولفیت سدیم از عصارههای تخمیری به صورت بیسولفیت جدا و استخراج نمود. در تخمیر الکلی به ازای مصرف هر مول گلوکز دو مول NADPH2 دو مول ATP و دو مول اسید پیروویک حاصل میشود.
در دومین مرحله تخمیر که تبدیل اسیدپیروویک به الکل اتیلیک است N ADH2 حاصل از مسیر گلیکولیز مصرف و تبدیل شده ، از تمام واکنشها فقط دومول ATP که حاصل از فسفریلاسیونهای وابسته به متابولیتهای این مرحله است باقی خواهد ماند واکنش کلی تبدیل گلوکز به الکل اتیلیک بطور خلاصه عبارت است از:
C6H12O62CH3CH2OH+2CO2 + 2ATP
بازده نظری تخمیر در حدود 44% و کمی بیش از بازده تنفس است. تجزیه گلوکز در واکنشهای تخمیری ناقص بوده از آن فقط 2 مول ATP حاصل میشود. در فرآیندهای تنفس تجزیه گلوکز بطور کامل صورت گرفته ، 36 مول ATP از آن نتیجه میشود.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 228 تاريخ : جمعه 19 تير 1388 ساعت: 19:18
مجموعه مشعل پالایشگاه واحدی است که جهت ایمن سازی محیط پالایشگاه و واحدهای بهره برداری طراحی و نصب شده است.
کاربرد اساسی آن مهار کردن و به کنترل درآوردن شرایط غیرقابل کنترلی است که دراثربالا رفتن بیش ازحد مجازعملیاتی دردستگاههای پالایش بوجود می آید. کنترل فوق از طریق تخلیه گازمازاد واحدها به شبکه مشعل انجام می گیرد.
مجموعه مشعل پالایشگاه واحدی است که جهت ایمن سازی محیط پالایشگاه و واحدهای بهره برداری طراحی و نصب شده است.
کاربرد اساسی آن مهار کردن و به کنترل درآوردن شرایط غیرقابل کنترلی است که دراثربالا رفتن بیش ازحد مجازعملیاتی دردستگاههای پالایش بوجود می آید. کنترل فوق از طریق تخلیه گازمازاد واحدها به شبکه مشعل انجام می گیرد.
این مجموعه شامل قسمتهای زیر می باشد:
1. لوله های رابط واحد
2. لوله اصلی (BLOW DOWN) مشعل که از محوطه بارگیری گاز مایع شروع شده و تا ستونهای مشعل امتداد دارد.
3. ظروف مایع گیر بین راهی (K.O.DROM)
4. تلمبه های تخلیه مایعات جمع شده در ظروف بین راهی
5. ستونهای اصلی مشعلها ME-2503 , ME-2502 , ME-2501
6. دستگاه جرقه زن الکتریکی برای روشن کردن مشعلها
خروجی تمام شیرهای ایمنی، لوله های تخلیه(DRAIN) و تهویه (VENT) ظروف برج ها، تلمبه ها ،کمپرسورها ،اعم از گازی یا مایع(به استثناء آب ،بخار،هوای فشرده، ازت و بعضی از هیدروکربورهای سبک که به هوای آزاد تخلیه می شوند) توسط لوله های تخلیه فشار هر واحد جمع آوری شده به لوله اصلی مشعل منتقل می گردند.
قسمت عمده مایعات همراه با گازها در ظروف مایع گیر بین راهی جداشده و گازها وارد محفظه آب بندی در پائین مشعل می گردند،پس از شستشو و حذف ذرات و مایعات احتمالی توسط آب برای سوختن به بالای مشعل هدایت و درتاج (TIP) مشعل می سوزند.
برای کنترل فشار واحدهای آب ترش،آمین و گوگرد که گازهای اسیدی محتوی H2S تولید می کند یک سیستم مشعل مخصوص (ME-2503) ACID FLARE طراحی و ساخته شده است که به موزات مشعلهای اصلی کشیده شده و بدنه مشعل شرقی ME-2501چسبیده است.
سیستم مشعل پالایشگاه از محوطه مخازن و بارگیری گاز مایع با یک لوله 20 اینچ شروع می شود و به ابتدای این لوله یک لوله 2 اینچ ازسوخت گازFUEL GAS جهت تأمین فشار مثبت در سیستم و رانش گازها به طرف مشعل و روشن نگه داشتن مشعل درهنگامی که میزان تخلیه مشعل کمترازحد مورد نیاز طراحی مشعل باشد تعبیه شده است.
مقداراین گازباید به اندازه ای باشد که بتواند مواد داخل لوله را به میزان حدأقل 0.4 متربرثانیه به جلو براند و از ایجاد خلأ و پس زدن شعله به داخل سیستم و خاموش شدن شعله مشعل جلوگیری کند.
این مقدار گاز تزریقی به وسیله دست تنظیم شده و توسط FI-25021.A اندازه گیری می شود.علاوه بر آن سیستم کنترل DCS پالایشگاه جهت مشاهده اپراتور روی CRT و دریافت نمودار ول گردیده است.
لوله اصلی مشعل بعد از جمع آوری گازهای تخلیه شده به آن در این قسمت با شیب 0.2% به ظرف V-2507 وارد می شود،این ظرف برخلاف سایر ظروف مایع گیر بین راهی مشعل فاقد چاهک آب گیر (BOOT) می باشد و درنتیجه تلمبه ای برای تخلیه مایعات ندارد،بنابراین مایعات جمع شده دراین ظرف به وسیله گرمای حاصله از یک مارپیچ بخارآب 4 bar تبخیر و از بالای آن خارج می شود و مایعات سنگین تر باقی مانده درمحوطه مخصوص ،به زمین تخلیه می شوند.
این ظرف جهت کنترل سطح مایع به آب نما LEVEL GAUGE و سوئیچ هشداردهنده مجهز بوده و در موقع بالا رفتن سطح مایع ازطریق سیستم کنترل DCS توسط (ALARM) روی CRT هشدار می دهد.
گازها و مایعات تبخیر شده از بالای V-2507 خارج شده همراه گاز رانشی (PURGEGAS) توسط یک لوله 20" به لوله تخلیه فشار واحد تقطیر مرتبط می گردند. شیب این لوله به طرف V-2503 بوده گازهای دریافتی از واحدهای کنترل 1 (تقطیر کاهش گرانروی،گاز مایع و سوخت گاز)را به داخل این ظرف هدایت می کند،ظرف مایع گیر V-2503 کلیه تجهیزات V-2507 را داشته وعلاوه برآن دارای چاهک مایع گیر و تلمبه تخلیه P-2503 می باشد که سوئیچ آن درای دو حالت MAN-AUTO می باشد که معمولاً در حالت AUTO قرار دارد و درآن حالت اگرسطح مایع در V-2503 بالا بیاید،LSH-25002 تلمبه P-2503 را روشن می کند و وقتی سطح مایع پائین بیاید SL-25003 تلمبه را به حالت خودکاراز سرویس خارج می نماید.
مایعات تلمبه شده به مخزن ضایعات سبک پالایشگاه COLD SLOPSTK هدایت می گردد. گازهای خروجی از V-2503 با جریان گازهای جمع آوری شده در واحدهای تبدیل کاتالیستی CCR هیدروژن و هیدروکراکر را دریافت می نماید و وارد V-2505 می شود.
V-2505 و تلمبه تخلیه مایعات آن مشابه V-2503می باشد چون هیدروکراکردرفشار بالا کار می کند برای آن یک لوله تخلیه فشار اضطراری جداگانه ازمسیرعادی کشیده است تا در هنگام لزوم برای تخلیه فشارسریع واحد هیدروکراکر استفاده شود.
گازهای خروجی از V-2505 و V-2503 با هم مخلوط شده و قبل ازورود به ظروف مایع گیر محوطه مشعل V-2503.2505 لوله 12" تخلیه مشعل واحدهای منطقه ج به آن تزریق می گردد.
ظروف V-2502 و V-2501 خارج ازمحوطه خطرناک مشعل قراردارند وهرکدام دارای ظروف قبلی جهت کنترل سطح مایع می باشند.
تلمبه های P-2501A/B مربوط به V-2502 بوده و مایعات جمع شده در این ظروف را به مخازن ضایعات سرد پالایشگاه می فرستد. این تلمبه ها دارای سوئیچ های انتخابی برای تنظیم حالت MAN یا AUTO می باشد.
اگر آنها به صورت AUTO قرار داده شوند مستقیم از LEVEL SWITCH های ظروف مربوط فرمان گرفته خاموش یا روشن می شوند واگردرحالت MAN باشند می توان آنها را توسط HS-25007 و یا HS-25006 از روی CRT اتاق کنترل خاموش یا روشن کرد.

مجموعه مشعل پالایشگاه دارای دو ستون اصلی FLARE STACK به شماره های ME-2501ME-2502, می باشد که قطرآنها 25" و ارتفاع آنها 83 مترمی باشدوهمچنین یک ستون مشعل برای گازهای اسیدی به قطر 16" و ارتفاع 83 متر برای گازهای اسیدی می باشند که به ستون مشعل شرقی ME-2501 چسبیده است.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 224 تاريخ : جمعه 19 تير 1388 ساعت: 19:6
مبتكران ايراني موفق به ساخت چنگي شدند كه براساس قطع شدن پرتوهاي ليزر توسط دست انسان آهنگ مينوازد.
حنيفيان، از مبتكران اين طرح در گفتوگو با ايسنا اظهار كرد: در قسمت بالاي اين چنگ، 15 ليزر نصب شده است كه به سمت پايين مي تابند و در قسمت پايين روبه روي هر ليزر، يك سنسور نوري قرار دارد.
وي افزود: زماني كه مسير ليزر با دست انسان قطع ميشود، سنسور پاييني به وسيله مداري كه به ارگ وصل است فرمان نواختن نت مربوطه را صادر ميكند.
حنيفيان ضمن اشاره به عدم توانايي انسان در ديدن نور ليزر به علت مستقيم بودن آن، اظهار كرد: براي قابل رويت كردن نورهاي ليزر بايد محيط حالت غبار آلود و مه آلود داشته باشد، به همين دليل در قسمت بالاي اين چنگ تعدادي مه ساز نصب شده تا بتواند مه مصنوعي، جهت ديدن مسير ليزر توليد كند.
گفتني است، اين دستگاه جهت بازديد دانشآموزان و خانوادهها جهت ايجاد شوق و علاقه علمي در پاركهاي علمي تفريحي در اصفهان، مشهد، تهران و ... به نمايش عمومي گذاشته شده است.
برای مشاهده ی عکس هایی از چنگ به ادامه مطلب بروید ...
مبتكران ايراني موفق به ساخت چنگي شدند كه براساس قطع شدن پرتوهاي ليزر توسط دست انسان آهنگ مينوازد.
حنيفيان، از مبتكران اين طرح در گفتوگو با ايسنا اظهار كرد: در قسمت بالاي اين چنگ، 15 ليزر نصب شده است كه به سمت پايين مي تابند و در قسمت پايين روبه روي هر ليزر، يك سنسور نوري قرار دارد.
وي افزود: زماني كه مسير ليزر با دست انسان قطع ميشود، سنسور پاييني به وسيله مداري كه به ارگ وصل است فرمان نواختن نت مربوطه را صادر ميكند.
حنيفيان ضمن اشاره به عدم توانايي انسان در ديدن نور ليزر به علت مستقيم بودن آن، اظهار كرد: براي قابل رويت كردن نورهاي ليزر بايد محيط حالت غبار آلود و مه آلود داشته باشد، به همين دليل در قسمت بالاي اين چنگ تعدادي مه ساز نصب شده تا بتواند مه مصنوعي، جهت ديدن مسير ليزر توليد كند.
گفتني است، اين دستگاه جهت بازديد دانشآموزان و خانوادهها جهت ايجاد شوق و علاقه علمي در پاركهاي علمي تفريحي در اصفهان، مشهد، تهران و ... به نمايش عمومي گذاشته شده است.

برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 232 تاريخ : جمعه 19 تير 1388 ساعت: 19:4
به گزارش ايرنا به نقل از سايت ستاد ويژه توسعه فناوري نانو، اين گروه همچنين موفق شد ليزر بخار مس را به عنوان منبع ليزر جديدي در اين روش معرفي کند.
اين پژوهشگر افزود: از سوي ديگر، يک جمعکننده مسي آب خنک در انتهاي محفظه و درست خارج از فضاي دماي بالاي کوره براي جمع کردن نانولولهها پس از رشد تعبيه شده است.
محقق اين طرح تصريح کرد توجه به معرفي ليزر بخار مس به عنوان يک منبع جديد در سنتز نانولولههاي کربني در سطح جهان، اين تحقيق ثبت اختراع را دارد.
نتايج اين تحقيق در مجله Applied Physics A: Materials Science & Processing (جلد 94، صفحات 297-293، سال 2009) منتشر شده است.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 327 تاريخ : جمعه 19 تير 1388 ساعت: 19:2
فلز مادهای است که میتوان آن را صیقل داده و براق کرد، یا به طرحهای گوناگون در آورد و از آن مفتولهای سیمی ظریف تهیه کرد. فلز جسمی است که آزمایشهای مربوط به گرما و مهمتر از همه جریان الکتریکی را به خوبی هدایت میکند. فلزات با یکدیگر فرق زیادی دارند، از جمله در رنگ و سختی و نرمی ، تعدادی از آنها ممکن است به آسانی خم شده و یا خیلی محکم و مقاوم باشند.

فلز مادهای است که میتوان آن را صیقل داده و براق کرد، یا به طرحهای گوناگون در آورد و از آن مفتولهای سیمی ظریف تهیه کرد. فلز جسمی است که آزمایشهای مربوط به گرما و مهمتر از همه جریان الکتریکی را به خوبی هدایت میکند. فلزات با یکدیگر فرق زیادی دارند، از جمله در رنگ و سختی و نرمی ، تعدادی از آنها ممکن است به آسانی خم شده و یا خیلی محکم و مقاوم باشند.
امروزه ، بازتاب اثرات فلزات در زندگی انسان ، بقدری محسوس است که هر گاه از فلز نام میبریم ، ساختمانهای بدیع و آسمان خراشهای عظیم در برابر چشم مجسم میشود، همچنین هواپیماها و موشکهای غول پیکری به خاطر میآید که در دل آسمان و کهکشانها راه میپویند و با پرواز خود فاصله و زمان مسافرت را کوتاهتر ساخته ، انسان را در رسیدن به کرات دیگر یاری میکنند. راستی اگر فلز نبود، زندگی و تمدن بشری به چنین مرحلهای میرسید؟
گروهی از عناصر هستند که خواص مشترک معینی دارند. این مواد ، گرما و الکتریسیته را به خوبی هدایت میکنند، و به همین دلیل ظروف آشپزی و سیمهای برق از فلز ساخته می شود. فلزها همچنین محکماند و بآسانی میتوان آنها را شکل داد؛ به همین دلیل است که از آنها برای ساختن سازه هایی از قبیل پلها استفاده می شود. اگر چه شباهتهای زیادی بین فلزها وجود دارد، تفاوتهایی نیز دارند که مشخص میکند یک فلز تا چه حد برای یک کاربرد خاص مناسب است.
از 109 عنصری که امروزه شناخته شده است، 87 عنصر فلز است. از فلزها بندرت به شکل خالص استفاده میشود؛ معمولا با مخلوط کردن یک فلز با فلزهای دیگر یا غیر فلزها آلیاژی از آن را تشکیل میدهند.
شکل واقعی فلزات
شکل واقعی فلزات به اندازه یون و تعداد الکترونهایی که هر یون در حوزه اشتراکی دارد و انرژی یونها و الکترونها بستگی دارد. هر قدر فلز گرمتر شود این انرژی زیادتر خواهد شد. پس فلزات گوناگون ممکن است طرحهای گوناگونی به خود بگیرند. یک فلز ممکن است در حرارتهای مختلف ، طرحهای متنوعی را اختیار کند، اما در بیشتر آرایشها ، یونها کاملا پهلوی هم قرار دارند، و معمولا تراکم در فلزات زیادتر از دیگر مواد است.
اختلافات عمده فلزات و دیگر جامدات و مایعات
فلزات هادی خوب برق هستند. چون الکترونهای آنها برای حرکت مانعی ندارند. همه فلزات جامد و مایع گروهی الکترون آزاد دارند، طبعا همه فلزات هادیهای خوب الکتریسیته میباشند. به این سبب فلزات از دیگر گروههای عناصر ، کاملا متفاوت دارد.
اختلاف عمده فلزات و دیگر جامدات و مایعات ، در توانایی هدایت گرما و الکتریسیته است. هادی خوب آزمایشهای مربوط به گرما جسمی است که ذرات آن طوری تنظیم شوند که بتوانند آزادانه نوسان یافته و به ذرات مجاور خود نیز امکان نوسان آزاد را بدهند. "گرم شدن" همان نوسانات سریع یونها و الکترونها است. در فلزات چون گروه الکترونها ، غبار مانند یونها را احاطه میکنند، طبعا هادیهای خوبی برای حرارت هستند (رسانش گرمایی فلزات).
مقاومت فلز
مقصود آن مقدار باری است که فلز میتواند تحمل کرده ، نشکند. بسیاری از فلزات ، وقتی گرم هستند، اگر تحت فشار قرار گیرند، شکل خود را زیادتر از موقعی که سرد هستند، تغییر میدهند. بسیاری از فلزات در زیر فشار متغییر مانند نوسانات ، آسانتر از موقعی که سنگین باری را تحمل میکنند، میشکنند.
چرا فلزات ظاهر درخشنده یا براق دارند؟
دلیل اول آن است که با طرح ریزی و براق کردن صحیح میتوان فلزات را به شکل خیلی صاف تهیه کرد. گر چه آنها نیز تصاویر را خوب منعکس میکنند، ولی ظاهر سفید و درخشان بیشتر قطعات فلزی صیقلی شده را ندارند. بطور کلی جلا و درخشندگی فلز بستگی دارد به گروه الکترونهای آن دارد.
الکترونها میتوانند هر نوع انرژی را که به روی فلزات میافتد جذب کنند؛ زیرا در حرکت آزاد هستند. بیشتر انرژی الکترونها از تابش نوری است که به آنها میافتد، خواه نور آفتاب باشد یا نور برق. اکثر فلزات همه انرژی جذب شده را پس میدهند، به همین دلیل ، نه تنها درخشان بلکه سفید به نظر میآیند.
چرا فلزات تغییر شکل میدهند؟
بسیاری از فلزات در حرارت ویژهای ، آرایش یونهای خود را تغییر میدهند. با تغییر ترتیب آرایش یونهای بسیاری از خصوصیات دیگر فلز نیز دگرگون میشود و ممکن است فلز کم و بیش شکننده ، قردار ، بادوام و قابل انحنا شود یا اینکه انجام کار با آن آسان گردد. بسیاری از فلزات در هنگام سرد بودن ، به سختی تغییر شکل میپذیرند. بیشتر فلزات جامد را به زحمت میتوان در اثر کوبیدن به صورت ورقه و مفتولهای سیم در آورده ، ولی اگر فلز گرم شود، انجام هر دو آسان است.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 262 تاريخ : پنجشنبه 18 تير 1388 ساعت: 10:22
متداولترین مقیاس الکترونگاتیویته
مقیاس نسبی الکترونگاتیوی پاولینگ ، متداولترین مقیاس و مبتنی بر مقادیر تجربی انرژیهای پیوندی است. مقدار انرژی اضافی که از جاذبه متقابل بارهای جزئی б+ و б- اضافه بر انرژی پیوند کووالانسی آزاد میشود، به قدر مطلق б و به تفاوت الکترونگاتیوی دو عنصر پیوند شده بستگی دارد. در محاسبات الکترونگاتیوی تنها تفاوت الکترونگاتیویته عناصر تعیین میشود. برای بنا کردن یک مقیاس ، به اتم F (الکترونگاتیوترین عنصر) بطور دلخواه عدد 4 نسبت داده شده است.
متداولترین مقیاس الکترونگاتیویته
مقیاس نسبی الکترونگاتیوی پاولینگ ، متداولترین مقیاس و مبتنی بر مقادیر تجربی انرژیهای پیوندی است. مقدار انرژی اضافی که از جاذبه متقابل بارهای جزئی б+ و б- اضافه بر انرژی پیوند کووالانسی آزاد میشود، به قدر مطلق б و به تفاوت الکترونگاتیوی دو عنصر پیوند شده بستگی دارد. در محاسبات الکترونگاتیوی تنها تفاوت الکترونگاتیویته عناصر تعیین میشود. برای بنا کردن یک مقیاس ، به اتم F (الکترونگاتیوترین عنصر) بطور دلخواه عدد 4 نسبت داده شده است.
مقیاس الکترونگاتیوی پاولینگ ، متداولترین مقیاس و مبتنی بر مقادیر تجربی انرژیهای پیوند است. مثلا انرژی پیوند Br-Br ، انرژی لازم برای تفکیک مولکول Br2 به اتمهای Br است. برای تفکیک یک مول از مولکولهای Br2 به اندازه 46+ کیلو کالری انرژی لازم است. انرژی پیوند H-H برابر 104+ کیلو کالری بر مول است.
تعاریف مختلف الکترونگاتیویته
الکترونگاتیویته ، در روشهای متفاوتی تعریف شده است که برخی از آنها به اختصار توضیح داده میشود.
الکترونگاتیویته پاولینگ
انرژی اضافی پیوند A-B نسبت به متوسط انرژی پیوندهای A-A و B-B میتواند به حضور سهم یونی در پیوند کوالانسی نسبت داده شود. اگر انرژی پیوند A-B بطور قابل ملاحظه ای از متوسط پیوندهای غیر قطبی A-A و B-B متفاوت باشد، میتوان فرض کرد که سهم یونی در تابع موج و بنابراین اختلاف بزرگ در الکترونگاتیوی وجود دارد.
الکترونگاتیویته آلرد_روکر
در این تعریف ، الکترونگاتیویته توسط میدان الکتریکی بر سطح اتم مشخص میشود. بنابرین الکترون در یک اتم بار موثر هستهای را احساس میکند. بر طبق این تعریف ، عناصری با الکترونگاتیویته بالا آنهایی هستند که با بار هستهای موثر بزرگ و شعاع کوالانسی کوچک ، این عناصر در نزدیکی فلوئور قرار دارند.
الکترونگاتیویته مولیکن
مولیکن تعریف خود را بر پایه دادههای طیفهای اتمی نهاد. او فرض کرد که توزیع دوباره الکترون در طی تشکیل تر کیب به گونهای است که در آن یک اتم به کاتیون (توسط ار دست دادن الکترون) و اتم دیگر به آنیون (توسط گرفتن الکترون) تبدیل میشود.
اگر یک اتم دارای انرژی یونیزاسیون بالا و الکترونخواهی بالا باشد، احتمالا در هنگام تشکیل پیوند ، الکترونها را به سوی خود میکشد. بنابراین بعنوان الکترونگاتیو شناخته میشود. از طرف دیگر اگر انرژی یونش و الکترونخواهی آن ، هر دو کوچک باشد تمایل دارد تا الکترون از دست بدهد. بنابراین به عنوان الکترو پوزیتیو طبقه بندی میشود.
این مشاهدات تعریف مولیکن را به عنوان مقدار متوسط انرژی یونش و الکترونخواهی عنصر معرفی میکند.
تغییرات الکترونگاتیویته عناصر
الکترونگاتیویته عناصر با افزایش تعداد الکترونهای والانس و همچنین کاهش اندازه اتم افزایش مییابد و در هر دوره از جدول تناوبی از چپ به راست و در هر گروه از پایین به بالا افزایش مییابد. فلزات ، جاذبه کمی برای الکترونهای والانس دارند و الکترونگاتیوی آنها حاکم است، ولی نافلزات ، به استثنای گازهای نجیب ، جاذبه قوی برای اینگونه الکترونها دارند و الکترونگاتیوی آنها زیاد است.
بطور کلی ، الکترونگاتیوی عناصر در هر دوره از چپ به راست (با افزایش تعداد الکترونهای والانس) و در هر گروه از پایین به بالا (با کاهش اندازه اتم) افزایش مییابد. بنابراین ، الکترونگاتیوترین عناصر ، در گوشه بالایی سمت راست جدول تناوبی (بدون در نظر گرفتن گازهای نجیب) و عناصری که کمترین الکترونگاتیوی را دارند، در گوشه پایینی سمت چپ این جدول قرار دارند. این سیر تغییرات ، با سیر تغییرات پتانسیل یونش و الکترونخواهی عناصر در جدول تناوبی همجهت است.
مفهوم الکترونگاتیوی
مفهوم الکترونگاتیوی گرچه مفید است، ولی دقیق نیست. روشی ساده و مستقم برای اندازه گیری خاصیت الکترونگاتیویته وجود ندارد و روشهای گوناگون برای اندازه گیری آن پیشنهاد شده است. در واقع چون این خاصیت علاوه بر ساختمان اتم مورد نظر به تعداد و ماهیت اتمهای متصل به آن نیز بستگی دارد، الکترونگاتیوی یک اتم نامتغیر نیست.
انتظار میرود که الکترونگاتیوی فسفر در PCl3 با الکترونگاتیوی آن در PCl5 تفاوت داشته باشد. از اینرو ، این مفهوم را تنها بایستی نیمهکمی تلقی کرد. بنابراین میتوان گفت که قطبی بودن مولکول HCl ناشی از اختلاف بین الکترونگاتیوی کلر و هیدروژن است چون کلر الکترونگاتیوتر از هیدروژن است، آن سر مولکول که به کلر منتهی میشود، سر منفی دو قطبی است.
توجیه پیوند یونی با خاصیت الکترونگاتیویته
پیوند یونی بین غیرفلزات وقتی تشکیل میشود که اختلاف الکترونگاتیوی آنها خیلی زیاد نباشد. در اینگونه موارد، اختلاف الکترونگاتیوی عناصر نشان دهنده میزان قطبی بودن پیوندهای کووالانسی است. اگر اختلاف الکترونگاتیوی صفر یا خیلی کوچک باشد، میتوان گفت که پیوند اساسا غیر قطبی است و اتمهای مربوط ، سهم مساوی یا تقریبا مساوی در الکترونهای پیوند دارند.
هر چقدر اختلاف الکترونگاتیوی بیشتر باشد پیوند کووالانسی قطبیتر خوهد بود (پیوند در جهت اتم الکترونگاتیوتر قطبی میشود). بنابراین با توجه به مقادیر الکترونگاتیوی میتوان پیشگویی کرد که HF قطبیترین هیدروژن هالیدها است و انرژی پیوندی آن بیشتر از هر یک از این ترکیبات است. البته نوع پیوندی که بین دو فلز تشکیل میشود، پیوند فلزی و در آن اختلاف الکترونگاتیوی نسبتا کم است.
کاربردهای الکترونگاتیویته
میتوان برای تعیین میزان واکنش پذیری فلزات و غیر فلزات بکار برد.
میتوان برای پیشبینی خصلت پیوندهای یک ترکیب بکار برد. هرچه اختلاف الکترونگاتیوی دو عنصر بیشتر باشد، پیوند بین آنها قطبیتر خواهد بود. هرگاه اختلاف الکترونگاتیوی دو عنصر در حدود 1.7 باشد، خصلت یونی نسبی پیوند بیش از 50% است.
اگر اختلاف الکترونگاتیوی صفر و یا خیلی کوچک باشد، پیوند غیر قطبی است. هرچه اختلاف الکترونگاتیوی بیشتر باشد، پیوند کووالانسی قطبیتر خواهد بود. در این پیوندها ، اتمی که الکترونگاتیوی بیشتری دارد، بار منفی جزئی را خواهد داشت.
با استفاده از مقادیر الکترونگاتیوی میتوان نوع پیوندی را که یک ترکیب ممکن است داشته باشد، پیشبینی کرد. وقتی دو عنصر با اختلاف الکترونگاتیوی زیاد با یکدیگر ترکیب می شوند، یک ترکیب یونی حاصل میشود. مثلا اختلاف الکترونگاتیوی سدیم و کلر 2.1 است و NaCl یک ترکیب یونی است.
آیا الکترونگاتیوی یک عنصر همیشه ثابت است؟
مفهوم الکترونگاتیوی غیر دقیق است. زیرا این خاصیت نه تنها به ساختمان اتم مورد بحث بستگی دارد، بلکه تعداد و ماهیت اتمهای دیگری که به اتم مزبور پیوند داده شدهاند نیز در آن دخالت دارد. بنابراین الکترونگاتیوی یک عنصر همیشه ثابت نیست مثلا الکترونگاتیوی فسفر در ترکیب (PCl3) متفاوت از الکترونگاتیوی آن در ترکیب (PCl5) است.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 260 تاريخ : پنجشنبه 18 تير 1388 ساعت: 10:19
پلی اتیلن یا پلی اتن یکی از سادهترین و ارزانترین پلیمرها است. پلی اتیلن جامدی مومی و غیر فعال است. این ماده از پلیمریزاسیون اتیلن بدست میآید و بطور خلاصه بصورت PE نشان داده میشود. مولکول اتیلن دارای یک بند دو گانه C=C است. در فرایند پلیمریزاسیون بند دو گانه هر یک از مونومرها شکسته شده و بجای آن پیوند سادهای بین اتمهای کربن مونومرها ایجاد میشود و محصول ایجاد شده یک درشتمولکول است.
تاریخچه تولید پلی اتیلن
پلی اتیلن اولین بار بطور اتفاقی توسط شیمیدان آلمانی "Hans Von Pechmanv" سنتز شد. او در سال 1898 هنگام حرارت دادن دی آزومتان ، ترکیب مومی شکل سفیدی را سنتز کرد که بعدها پلی اتیلن نام گرفت. اولین روش سنتز صنعتی پلی اتیلن بطور تصادفی توسط "ازیک ناوست" و "رینولرگیسون" ( از شیمیدانهای ICI ) در 1933 کشف شد. این دو دانشمند با حرارت دادن مخلوط اتیلن و بنزالدئید در فشار بالا ، مادهای موممانند بدست آوردند.
علت این واکنش وجود ناخالصیهای اکسیژندار در دستگاههای مورد استفاده بود که بعنوان ماده آغازگر پلیمریزاسیون عمل کرده بود. در سال 1935 "مایکل پرین" یکی دیگر از دانشمندهای ICI این روش را توسعه داد و تحت فشار بالا پلیاتیلن را سنتز کرد که این روش اساسی برای تولید صنعتی LDPE در سال 1939 شد.
پلی اتیلن یا پلی اتن یکی از سادهترین و ارزانترین پلیمرها است. پلی اتیلن جامدی مومی و غیر فعال است. این ماده از پلیمریزاسیون اتیلن بدست میآید و بطور خلاصه بصورت PE نشان داده میشود. مولکول اتیلن دارای یک بند دو گانه C=C است. در فرایند پلیمریزاسیون بند دو گانه هر یک از مونومرها شکسته شده و بجای آن پیوند سادهای بین اتمهای کربن مونومرها ایجاد میشود و محصول ایجاد شده یک درشتمولکول است.
تاریخچه تولید پلی اتیلن
پلی اتیلن اولین بار بطور اتفاقی توسط شیمیدان آلمانی "Hans Von Pechmanv" سنتز شد. او در سال 1898 هنگام حرارت دادن دی آزومتان ، ترکیب مومی شکل سفیدی را سنتز کرد که بعدها پلی اتیلن نام گرفت. اولین روش سنتز صنعتی پلی اتیلن بطور تصادفی توسط "ازیک ناوست" و "رینولرگیسون" ( از شیمیدانهای ICI ) در 1933 کشف شد. این دو دانشمند با حرارت دادن مخلوط اتیلن و بنزالدئید در فشار بالا ، مادهای موممانند بدست آوردند.
علت این واکنش وجود ناخالصیهای اکسیژندار در دستگاههای مورد استفاده بود که بعنوان ماده آغازگر پلیمریزاسیون عمل کرده بود. در سال 1935 "مایکل پرین" یکی دیگر از دانشمندهای ICI این روش را توسعه داد و تحت فشار بالا پلیاتیلن را سنتز کرد که این روش اساسی برای تولید صنعتی LDPE در سال 1939 شد.
استفاده از انواع کاتالیزورها در سنتز پلیاتیلن
اتفاق مهم در سنتز پلی اتیلن ، کشف چندین کاتالیزور جدید بود که پلیمریزاسیون اتیلن را در دما و فشار ملایمتری نسبت به روشهای دیگر امکانپذیر میکرد. اولین کاتالیزور کشف شده در این زمینه تری اکسید کروم بود که در 1951 ، "روبرت بانکس" و "جان هوسن" در شرکت فیلیپس تپرولیوم آنرا کشف کردند. در 1953 ، "کارل زیگلر" شیمیدان آلمانی سیستمهای کاتالیزور شامل هالیدهای تیتان و ترکیبات آلی آلومینیومدار را توسعه داد.
این کاتالیزورها در شرایط ملایمتری نسبت به کاتالیزورهای فیلیپس قابل استفاده بودند و همچنین پلی اتیلن یک آرایش (با ساختار منظم) تولید میکردند. سومین نوع سیستم کاتالیزوری استفاده از ترکیبات متالوسن بود که در سال 1976 در آلمان توسط "والتر کامینیکی" و "هانس ژوژسین" تولید شد. کاتالیزورهای زیگلر و متالوسن از لحاظ کارکرد بسیار انعطافپذیر هستند و در فرایند کوپلیمریزاسیون اتیلن با سایر اولفینها که اساس تولید پلیمرهای مهمی مثل VLDPE و LLDPE و MDPE هستند، مورد استفاده قرار میگیرند.
اخیرا کاتالیزوری از خانواده متالوینها با قابلیت استفاده بالا برای پلیمریزاسیون پلی اتیلن به نام زیرکونوسن دی کلرید ساخته شده است که امکان تولید پلیمر با ساختار بلوری (تک آرایش) بالا را میدهد. همچنین نوع دیگری از کاتالیزورها به نام کمپلکس ایمینوفتالات با فلزات گروه ششم مورد توجه قرار گرفته است که کارکرد بالاتری نسبت به متالوسنها نشان میدهند.
انواع پلی اتیلن
طبقهبندی پلی اتیلنها بر اساس دانسیته آنها صورت میگیرد که در مقدار دانسیته اندازه زنجیر پلیمری و نوع و تعداد شاخههای موجود در زنجیر دخالت دارد.
HDPE (پلیاتیلن با دانسیته بالا) این پلیاتیلن دارای زنجیر پلیمری بدون شاخه است بنابراین نیروی بین مولکولی در زنجیرها بالا و استحکام کششی آن بیشتر از بقیه پلی اتیلنها است. شرایط واکنش و نوع کاتالیزور مورد استفاده در تولید پلی اتیلن HDPE موثر است. برای تولید پلیاتیلن بدون شاخه معمولا از روش پلیمریزاسیون با کاتالیزور زیگلر- ناتا استفاده میشود.
LDPE (پلیاتیلن با دانسیته پایین) این پلی اتیلن دارای زنجیری شاخهدار است بنابراین زنجیرهای LDPE نمیتوانند بخوبی با یکدیگر پیوند برقرار کنند و دارای نیروی بین مولکولی ضعیف و استحکام کششی کمتری است. این نوع پلی اتیلن معمولا با روش پلیمریزاسیون رادیکالی تولید میشود. از خصوصیات این پلیمر ، انعطافپذیری و امکان تجزیه بوسیله میکروارگانیسمها است.
LLDPE (پلی اتیلن خطی با دانسیته پایین)
این پلی اتیلن یک پلیمر خطی با تعدادی شاخههای کوتاه است و معمولا از کوپلیمریزاسیون اتیلن با آلکنهای بلند زنجیر ایجاد میشود.
MDPE
پلی اتیلن با دانسیته متوسط است.
کاربرد پلیاتیلن کاربرد فراوانی در تولید انواع لوازم پلاستیکی مورد استفاده در آشپزخانه و صنایع غذایی دارد. از LDPE در تولید ظروف پلاستیکی سبک و همچنین کیسههای پلاستیکی استفاده میشود. HDPE ، در تولید ظروف شیر و مایعات و انواع وسایل پلاستیکی آشپزخانه کاربرد دارد. در تولید لولههای پلاستیکی و اتصالات لولهکشی معمولا از MDPE استفاده میکنند.
LLDPE بدلیل بالا بودن میزان انعطافپذیری در تهیه انواع وسایل پلاستیکی انعطافپذیر مانند لولههایی با قابلیت خم شدن کاربرد دارد. اخیرا پژوهشهای فراوانی در تولید پلی اتیلنهایی با زنجیر بلند و دارای شاخههای کوتاه انجام شده است. این پلی اتیلنها در اصل HDPE با تعدادی شاخههای جانبی هستند. این پلی اتیلنها ترکیبی ، استحکام HDPE و انعطافپذیری LDPE را دارند.

گزارش کار اندازه گيري دبي به كمك وسايل اندازه گيري - جمعه سیزدهم مرداد 1391
کلمه شیمی یعنی چی؟؟ - جمعه سیزدهم مرداد 1391
زندگینامه آلبرت انیشتین+ عکس رنگی! - جمعه سیزدهم مرداد 1391
معرفی سایتی در زمینه مواد شیمیایی - جمعه سیزدهم مرداد 1391
معرفی کامل رشته شیمی محض و کاربردی - جمعه سیزدهم مرداد 1391
دانلود کتاب تشریح مسائل مکانیک سیالات استریتر - پنجشنبه دوازدهم مرداد 1391
راهنمای حفظ کردن آسان جدول تناوبی - سه شنبه دهم مرداد 1391
دانلود و آموزش نرم افزار Chem 4D Demo - سه شنبه دهم مرداد 1391
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 252 تاريخ : دوشنبه 15 تير 1388 ساعت: 22:0
پلیمرها یا بسپارها ، ترکیباتی هستند که از بهم پیوستن چندین مولکول منومر بوجود میآیند. پلیمرها را به طرق مختلف طبقهبندی میکنند. یکی از روشهای تقسیم بندی پلیمرها ، تقسیم بندی از نظر خواص است. پلیمرها از نظر خواص به سه دسته عمده تقسیم بندی میشوند.
توموپلاستها
ترموپلاستها ، پلیمرهایی هستند که در اثر فشار ، تغییر شکل (Deformation) میدهند و بعد از حذف نیروی خارجی ، این تغییر شکل ، همچنان باقی میماند. به عبارت دیگر این پلیمرها ، خاصیت پلاستیسیتی دارند. این پلیمرها در اثر گرما بتدریج نرم میشوند. با افزایش دما به حالت مذاب در میآیند. بعد از حذف گرما به حالت فیزیکی جامد خود تبدیل میشوند. این خصلت ، کاربرد صنعتی این نوع پلیمرها را تضمین میکند.
اگر ترموپلاستیکی را به صورت پودر یا حلقههای کوچک در آوریم و سپس حرارت دهیم، ابتدا نرم و سپس مذاب و ویسکوز میشود و اگر آنرا در قالب بگیریم، شکل قالب را به خود میگیرد و این علت کاربرد بسیار زیاد این مواد است.
پلیمرها یا بسپارها ، ترکیباتی هستند که از بهم پیوستن چندین مولکول منومر بوجود میآیند. پلیمرها را به طرق مختلف طبقهبندی میکنند. یکی از روشهای تقسیم بندی پلیمرها ، تقسیم بندی از نظر خواص است. پلیمرها از نظر خواص به سه دسته عمده تقسیم بندی میشوند.
توموپلاستها
ترموپلاستها ، پلیمرهایی هستند که در اثر فشار ، تغییر شکل (Deformation) میدهند و بعد از حذف نیروی خارجی ، این تغییر شکل ، همچنان باقی میماند. به عبارت دیگر این پلیمرها ، خاصیت پلاستیسیتی دارند. این پلیمرها در اثر گرما بتدریج نرم میشوند. با افزایش دما به حالت مذاب در میآیند. بعد از حذف گرما به حالت فیزیکی جامد خود تبدیل میشوند. این خصلت ، کاربرد صنعتی این نوع پلیمرها را تضمین میکند.
اگر ترموپلاستیکی را به صورت پودر یا حلقههای کوچک در آوریم و سپس حرارت دهیم، ابتدا نرم و سپس مذاب و ویسکوز میشود و اگر آنرا در قالب بگیریم، شکل قالب را به خود میگیرد و این علت کاربرد بسیار زیاد این مواد است.
الاستومرها
الاستومرها ، پلیمرهایی هستند که در اثر نیروی خارجی تغییر شکل پیدا میکنند. بعد از حذف نیرو ، تغییر شکل از بین میرود و دوباره به حالت اولیه باز میگردند. این پلیمرها در اثر گرما ، نرم میشوند، ولی برخلاف ترموستها (ترموپلاستیکها) به حالت ویسکوز یا مایع سیال در نمیآیند. موقعی که این پلیمرها در اثر حرارت نرم شدند، آنرا با اضافه کردن افزودنیهای مورد نیاز در داخل قالب پخت میکنند. عملیات پخت را Curing گویند.
ترموسیتینگها
این پلیمرها ، پلیمرهایی هستند که در اثر گرما نرم نمیشوند. بلکه با افزایش دما ، سختتر و محکمتر میشوند و با بالا رفتن بیشتر دما ، درجه سختی آنها افزایش مییابد. این پلیمرها برای قالب گیری ، درون قالب ریخته میشوند و قالب گیری میشوند. گاهی ممکن است فرایند پلیمریزاسیون نیز همزمان درون قالب انجام شود و بعد از پلمریزاسیون ، پلیمر شکل قالب را به خود میگیرد.
مقایسه ترموستها ، الاستومرها و ترموسیتینگها از نظر ساختمانی
ترموستها و الاستومرها ، پلیمرهای یکبعدی هستند. بنابراین در حلالهای مرسوم شیمیایی که بسته به نوع ساختمان پلیمر تعیین میشود، حل میگردند. اما ترموسیتینگها ، جزو پلیمرهای سه بعدی یا مشبک میباشند و بنابراین در هیچ حلالی حل نمیشوند.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 265 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:56
لاستیک طبیعی یا سنتزی معمولا به تنهایی قابل استفاده نیست خواص مطلوب نرمینگی ، کشسانی ، چقرمگی ، سختی یا نرمی ، مقاومت سایشی ، نفوذ ناپذیری و هزاران ترکیب مختلف از خواص بدست آمده ، آمیزه کار لاستیک ، تامین میشود. لاستیک مادهای بینهایت چقرمه است و به ماشین آلات سنگین نیاز دارد. مقادیر قابل توجه گرمای تولید شده در طول عملیات اختلاط ، خرد کردن ، آسیاب کردن و روزن رانی در هنگام ساخت لاستیک باید دفع و تحت کنترل داشت.
آمیزه کاری لاستیکها
در آمیزه کاری لاستیکها افزودنیهای شیمیایی بسته به مصرفشان به گروههای دسته بندی میشوند.
مواد ولکانشی :
معمولا ترکیبات گوگردی هستند که از واکنش آنها با بسپار مواد شبکهای بدست میآید و اتصالات شبکه از نوع است. اتصالات عرضی ممکن است مونو – ، دی - ، یا پلی سولفیدی باشند. نوع اتصال از طریق غلظت گوگرد ، تسریع کننده ، باز دارنده و دما تعیین میشود.
تسریع کنندهها :
ترکیباتی هستند که زمان لازم برای ولکانشی لاستیک را از چند ساعت به چند دقیقه کاهش میدهند. ضمنا به گوگرد کمتری نیاز است و محصول یکنواختتری هم بدست میآید. اغلب تسریع کنندهها نیتروژن و گوگرد دارند.
مواد ضد پیری یا ضد اکسندهها :
این مواد قطعات لاستیکی را از تهاجم اکسیژن و اوزون محافظت میکنند. این ترکیبات به عنوان ضد اکسنده ، ضد اوزون یا عوامل ضد ترک خمشی دسته بندی میشوند. عمل آنها به این صورت است که واکنشهای زنجیری رادیکالی را متوقف میکنند و بدین ترتیب مانع از تخریب پیشتر زنجیر می شوند. مواد صنعتی معمولا آمینی یا فنلی هستند. آمینها محافظهای قوی هستند و به شکل وسیع در تایر و سایر قطعات تیره مصرف میشوند.
نرمسازهای کاتالیزی یا مواد لختهزدا :
این مواد با کاهش گرانروی لاستیک فراورش آنرا آسان میکند. موقع اختلاط با لاستیک سبب شکست زنجیر و طبعا کاهش وزن مولکولی زیاد قابل استفادهاند.
پراکنهای بیاثر یا خنثی :
این مواد به مقدار زیاد به لاستیک اضافه میشوند. بعضی از آنها تنها برای سخت کردن یا نرم کردن فیزیکی است. خاک رس ، کربنات کلسیم ، خرده ذغال ، باریت و تقریبا گرد هر جامدی را میتوان به لاستیک افزود که در نتیجه آن کلیه خواص کشش کاهش مییابد. ولی در عین حال کاهش مییابد ولی در عین حال کاهش قیمت ، سخت مناسب ، فقط شکل ، رنگ و سایر خواص مطلوب از دیگر آثار آن است. اما گرد بعضی مواد بی شکل خصوصا دوده و سیلیس ، به طرز ناباورانهای سبب افزایش استحکام ، جهندگی ، مقاومت سایشی و سایر خواص مطلوب میشود و به همین سبب به تقویت کننده موسوماند.
فراوش پذیری با استفاده از لاستیک بازیافتی ، واکسها ، روغنها ، فاکتیس (روغنهای گیاهی و ولکانیده) و لاستیکهای معدنی (آسفالت ، قیر و هیدروکنهای سیر نشده و ولکانیده) یا از طریق واکنش شیمیایی روی مولکول ، کار مکانیکی ، گرما و خرد کردن بهبود می یابد. ساختار اسفنجی با افزودن بیکربنات سدیم ، کربنات سدیم ، کربنات آمونیوم و بیکربنات ، اوره یا ترکیبات آلی گاز زا به دست میآید. با افزایش قابل توجه و گوگرد و استفاده از پرکن در مقادیر زیاد به لاستیک سخت میتوان دست یافت.
روشها و مراحل ساخت لاستیک
غلتک زنی یا پوشش دهی :
یکی از ابتداییترین مصارف لاستیکها ، پوشش دهی پارچه برای ضد آب کردن آن بوده است. محلول یا بتونههای لاستیکی در حلالها را میتوان به سادگی روی پارچه پخش کرد. اما اگر از مواد لازم برای پخت و کنترل خواص استفاده نشود نتایج کاملا نامطلوبی به دست میآید. برای آغشته کردن پارچه به آمیزههای لاستیکی از روش غلتک زنی استفاده میشود، به این صورت که بر روی دستگاههای غلتک زن چند استوانهای آمیزه لاستیکی را تحت فشار به داخل پارچه نورد میکنند. نخ تایر مورد خاصی است که برای ساخت آن نخهای پنبه ، ریون ، نایلون یا پلی استر در آرایش موازن توسط لاستیک روی یک دستگاه غلتکزن به هم میچسبند.
قالب گیری :
آمیزههای خمیری لاستیکی را میتوان به هر شکلی قالبگیری و شکل آنها را با پخت در قالب تثبیت کرد. یک نمونه مناسب توپ تنیس است. یک نوع بسیار مرغوب و ارتجاع پذیر لاستیک در قالبی که به شکل دو نیمه توپ است قالب گیری میشود. سپس این دو نیمه را به هم میچسبانند (با قرضی از مادهای شیمیایی گاز زا که در داخل قرار دارد) و پخت میکنند، بر روی این مغزی پارچه و الیاف پرزدار مناسب چسبانده میشود این ماده سازهای پیچیده که برای مصارف خیلی خشن مناسب است.
روزن رانی :
نوار درزگیر ، شیلنگ ، تیوپ ، نخ تایر ، واشر ، پروفیل و بسیاری دیگر از قطعات لاستیکی به تقلید از روش روزن رانی پلاستیکها ساخته و در طول همین عملیات یا بعدا ، پخت میشوند. تایر خودروها نمونه مناسبی است، مصرف عمده لاستیک در حمل و نقل است که به مصرف تایر میرسد. تایرهای امروزی ممکن است فاقد تیوپ باشند که در این صورت مجهز به لایهای محافظ هستند یا این که تیوپ روزن رانی شده از جنس لاستیک بوتیل در آنها قرار داده میشود. لاستیک بوتیل با اینکه بسیار بی اثر یا مرده است ولی در برابر عبور هوا مقاومت بسیار عالی از خود نشان می دهد. در خودروهای جدید ، لاستیک را علاوه بر استفاده در تایر در پروفیل پنجره ، نوار درزگیر ، برف پاک کن ، شاسی موتور ، صندلی و به عنوان صدا خفه کن نیز به کار میبرند. به طوری که در هر وسیله نقلیه چیزی حدود Kg 115 لاستیک به کار میرود.
آمیزههای شیرابهای
شیرابههای غلیظ امکان استفاده از لاستیک را در شکل مایع فراهم میکنند، به صورتی که میتوان عملیات پخش کردن ، رنگ کردن ، غوطه وری یا اسفنج سازی را روی آنها اجرا کرد. مواد پخت به شکل تعلیق اضافه میشوند ولی تقویت روی شیرابهها چندان موثر نیست. با اینکه تجارت مبلمان ، بالش و تشک اسفنجی به استفاده از لاستیکهای پلی اورتان و پلیاتر روی آورده ، ولی استفاده از شیرابهها رو به گسترش است.
لاستیکهای بازیافتی
لاستیک بازیافتی مادهای مفید در آمیزه کاری است که از قطعات لاستیکی ضایعاتی به دست میآید. این قطعات را خرد و سپس با اعمال روشهای توام شیمیایی ، مکانیکی و حلال ، لاستیک ، پارچه ، فلز و سایر اجزای آن را جدا می کنند. لاستیک بازیافتی تا حدی وابسپارش میشود. و در حد بالایی دوده (یا رنگدانه دیگر) ، خاکستر و روغن دارد. با افزودن این ماده به آمیزه لاستیکی ، فراروش آمیزه بهتر میشود و معمولا به عنوان یک ماده ضایعاتی ارزان در محصولات بسیار ارزان هم به کار میرود. تنها حدود 10 درصد لاستیکهای نو بازیافت میشوند.
افزایش اخیر قیمت انرژی سبب توجه به ضایعات تایر به عنوان سوخت شده است. از سوختن 1Kg لاستیک MJ 17.7 انرژی بدست میآید. در حالی که سوختن همین مقدار زغال سنگ ، MJ 26.5 انرژی میدهد. استفاد از خرده تایرهای مستعمل در آسفالت نسبت به آسفالت معمولی مزایای بیشماری دارد. با اجرای این فرآیند سوئدی ، عمر جادهها بیش از چهار برابر شده ، اصطکاک چرخ با سطح افزایش یافته ، صدا و براقی سطح هم کاهش یافته است.
مشتقات لاستیکی
از لاستیکها به ویژه لاستیک طبیعی به عنوان ماده اولیه در تولید انواع مشتقات لاستیکی استفاده شده است. صنایع پلاستیک در حال حاضر به این درست مواد شیمیایی لاستیکی روی آورده است، چون خود لاستیک یک مواد اولیه گران است. هالیدها با لاستیک در موضع پیوند دوگانهاش واکنش میدهند. محصول ، لاستیک کلردار (از برم و ید هم میتوان استفاده کرد) است که به عنوان افزودنی رنگ قابل استفاده و در مقابل مواد شیمیایی مقاوم است.
از عمل کلرید هیدروژن بر محلول لاستیک در بنزن ، مشتق هیدروکلرید لاستیک بدست میآید، که بدون شک از بسیاری جوانب با خود لاستیک تفاوت دارد. این ماده پلاستیکی چقرمه و شفاف است که از فیلم آن در بسته بندی استفاده میشود. مشتق هیدرو کلرید لاستیک در برابر مواد شیمیایی مقاوم ، فیلم نازک عالی بدست میدهد و ضمنا رنگ ، بو ، مزه هم ندارد. PVC ، پلی اتیلن ، پلی پروپیلن و پلاستیکهای جدیدتر کاربرد این مشتق گران را محدود کرده اند. از مخلوط لاستیکها و رزینها به وفور استفاده میرود. با افزودن لاستیک خواص ویژهای چون مقاومت ضربهای ، کش پذیری و جهندگی افزایش مییابد.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 213 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:53
تحمل وزن خودرو
کاهش ضربه ناشی از نیروهای وارده از طرف جاده
امکان ایجاد حرکت در جهت دلخواه
انتقال نیروی ترمز و یا شتابگیری به جاده
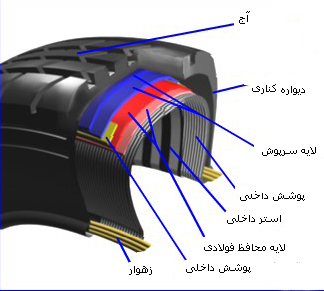
ساختمان تایر
آج تایر (tread) :
این قسمت به عنوان رابط بین سطح جاده و تایر ، با ترکیبی از لاستیکهای طبیعی و مصنوعی به عنوان لایه خارجی وظیفه محافظت از بدنه را در برابر سایش و صدمات احتمالی بر عهده دارد. طرحهای مختلف آج برای تخلیه بهتر آب از زیر تایر و افزایش قابلیت تایر در برخورد با شرایط گوناگون سطح جاده ساخته میشود. میتوان به طرحهای رگهای (Rib) ، عرضی (Lug) ، ترکیبی از عرضی و رگهای (Rib & Lug) و بلوکی (Block) اشاره کرد که هر یک مزایا و معایب خاص خود را دارند.
ضرورت وجود تایر در خودرو
تحمل وزن خودرو
کاهش ضربه ناشی از نیروهای وارده از طرف جاده
امکان ایجاد حرکت در جهت دلخواه
انتقال نیروی ترمز و یا شتابگیری به جاده
ساختمان تایر
آج تایر (tread) :
این قسمت به عنوان رابط بین سطح جاده و تایر ، با ترکیبی از لاستیکهای طبیعی و مصنوعی به عنوان لایه خارجی وظیفه محافظت از بدنه را در برابر سایش و صدمات احتمالی بر عهده دارد. طرحهای مختلف آج برای تخلیه بهتر آب از زیر تایر و افزایش قابلیت تایر در برخورد با شرایط گوناگون سطح جاده ساخته میشود. میتوان به طرحهای رگهای (Rib) ، عرضی (Lug) ، ترکیبی از عرضی و رگهای (Rib & Lug) و بلوکی (Block) اشاره کرد که هر یک مزایا و معایب خاص خود را دارند.برای مثال طرح رگهای در تایرها جهت استفاده در جادههای هموار برای حرکت سریع کاربرد دارد. مقاومت بالا در برابر لغزش و صدای کم از جمله ویژگیهای این طرح است. همچنین در مورد طرح عرضی میتوان گفت تایر با این آج نسبت به طرح رگهای ، کشش (traction) بهتری دارد. اما صدای آن زیاد است و مقاومت کمی هم در برابر لغزش دارد. این طرح بطور کلی بیشتر مناسب خودروهایی است که در مسیرهای ناهموار تردد میکنند. طرح بلوکی تایر نیز بیشتر در تایرهای ویژه برف کاربرد دارد، زیرا باعث کاهش لغزش در جادههای برفی میشود.
لایه های سرپوش (Cap plies) :
برخی تایرها با دارا بودن 2 یا چند لایه از جنس پلیاستر جهت نگه داشتن هر چه بهتر بقیه اجزای داخلی تایر خصوصا در سرعتهای بالا انتخاب مناسبی برای خودروهای پرسرعت خواهند بود.
تسمه محافظ (Belts) :
در تایرهای رادیال ، لایههای محافظ فولادی مانند حلقهای پیرامون تایر ، بین آج و بدنه قرار میگیرند. و علاوه بر ایجاد اتصال بین این دو قسمت و جذب ضربات ناشی از سطح جاده ، مانعی در مقابل سوراخ شدن بدنه ایجاد میکنند. البته در تایرهای بایاس پلای نیز لایههای محافظی از جنس نایلون و (بعضا در خودروهای سواری از جنس پلی استر) وجود دارد.
بدنه تایر (Car Cass):
بدنه متشکل از لایههایی از رشتههای مقاوم و مستحکم است که مجموعا قابلیت تحمل فشار داخلی تایر و همچنین جذب نیروهای وارده از سطح جاده را داراست. معمولا در خودروهای سواری جنس این لایه از الیاف پلیاستر است و در خودروهای سنگین از فولاد استفاده میشود. زاویه نصب این لایهها نسبت به محیط تایر در نوع رادیال بین 88 تا 90 درجه و در نوع بایاس پلای 30 تا 40 درجه است. استحکام یک تایر معمولی با تعداد لایههای بدنه توصیف میشود.
زهوار تایر (Bead Bundle) :
زهوار ، حلقهای از سیمهای فولادی با استحکام بالاست که با لاستیک پوشانده شدهاند و جهت حفظ وضعیت تایر در رینک و جلو گیری از خروج تایر بکار میرود.
دیوارههای کناری (Side Walls) :
پایداری جانبی تایر توسط این دیوارهها فراهم میشود و مشخصات تایر و نام سازنده آن نیز بر روی این قسمت نوشته میشود.
آستر داخلی تایر (Inner Liner) :
این لایه لاستیکی که جایگزینی برای تیوپ در تایرهای بدون تیوپ (Tubeless) است، جهت جلوگیری از نفوذ آزمایشهای مربوط به هوا به بیرون از تایر بکار میرود.
آخرین مرحله در تولید تایر
ابتدا طی مراحلی تمام اجزای مورد نیاز تایر تولید میشوند، ولی تا این مرحله آنها هنوز به صورت کاملا ثابت و محکم جایگیری نشدهاند، در ضمن هیچ گونه علامتی روی دیواره و یا طرحی روی آج آن وجود ندارد. در این مرحله به این مجموعه ، تایر نارس (Green tire) میگویند. در مرحله آخر تایر در ماشین کیورینگ (Curing machine) قرار میگیرد تا با کار کردی تقریبا مشابه فر اجاق گاز ، تمام علامتها و الگوی آج بوسیله قالبهای مربوط روی تایر ایجاد شود، گرمای بکار رفته در حین انجام این کار باعث محکم شدن هر چه بیشتر اتصال بین اجزای تایر میشود، کمی بعد از این جوشکاری (vulcanizing) و گذراندن مراحل بررسی کیفیت تایر تولیدی ، محصول آماده عرضه است.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 346 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:50
لاستیک به ماده مهم اقتصادی و راهبردی تبدیل شده است. در ایالات متحده ، مصرف سرانه لاستیک تقریبا 16.8 و در هندوستان تنها 0.22 است. صنایع حمل و نقل ، شیمیایی ، برق و الکترونیک و همچنین فضایی همگن از مصرف کنندگان اصلی لاستیک هستند. وقتی تولید لاستیک طبیعی (کائوچو) بدلیل تهاجم ژاپن به مناطق تولید لاستیک سنتزی کرد که به سرعت هم توسعه یافت. بطوری که در حال حاضر 88 درصد لاستیک مصرفی در ایالات متحده منشا سنتزی دارد. صنعت لاستیک موارد زیر را شامل میشود. تولید مواد اولیه لاستیکهای سنتزی ، انواع گوناگون لاستیک ، واردات لاستیک طبیعی ، تولید افزودنیهای لاستیک و نهایتا ساخت فراوردههای لاستیکی.
در ابتدای جنگ جهانی دوم وقتی تولید لاستیک طبیعی (کائوچو) بدلیل تهاجم ژاپن به مناطق تولید لاستیک متوقف شد. ایالات متحده اقدام به ساخت واحدهای تولید لاستیک سنتزی کرد که به سرعت هم توسعه یافت. به طوری که در حال حاضر 88 درصد لاستیک مصرفی در ایالات متحده منشا سنتزی دارد. بنابراین عموما لاستیکها را به دو نوع لاستیک طبیعی و لاستیک سنتزی طبقه بندی میکردند. امروزه لاستیکها را به روشهای مختلف دسته بندی میکنند.
لاستیک به ماده مهم اقتصادی و راهبردی تبدیل شده است. در ایالات متحده ، مصرف سرانه لاستیک تقریبا 16.8 و در هندوستان تنها 0.22 است. صنایع حمل و نقل ، شیمیایی ، برق و الکترونیک و همچنین فضایی همگن از مصرف کنندگان اصلی لاستیک هستند. وقتی تولید لاستیک طبیعی (کائوچو) بدلیل تهاجم ژاپن به مناطق تولید لاستیک سنتزی کرد که به سرعت هم توسعه یافت. بطوری که در حال حاضر 88 درصد لاستیک مصرفی در ایالات متحده منشا سنتزی دارد. صنعت لاستیک موارد زیر را شامل میشود. تولید مواد اولیه لاستیکهای سنتزی ، انواع گوناگون لاستیک ، واردات لاستیک طبیعی ، تولید افزودنیهای لاستیک و نهایتا ساخت فراوردههای لاستیکی.
در ابتدای جنگ جهانی دوم وقتی تولید لاستیک طبیعی (کائوچو) بدلیل تهاجم ژاپن به مناطق تولید لاستیک متوقف شد. ایالات متحده اقدام به ساخت واحدهای تولید لاستیک سنتزی کرد که به سرعت هم توسعه یافت. به طوری که در حال حاضر 88 درصد لاستیک مصرفی در ایالات متحده منشا سنتزی دارد. بنابراین عموما لاستیکها را به دو نوع لاستیک طبیعی و لاستیک سنتزی طبقه بندی میکردند. امروزه لاستیکها را به روشهای مختلف دسته بندی میکنند.
تاریخچه
کریستف کلمب دریافت که بومیان آمریکا با توپهای لاستیکی بازی می کنند. اشیای لاستیکی نیز از چاه مقدس مایا در یوکاتان بدست آمده بود. لاستیک ، تا جایی که میدانیم محصول سرزمین آمریکا است ولی تنها از طریق انتقال آن به خاور دور و کشت در آنجا به این حد توسعه یافته است. نام Rubber به معنی پاک کن را پریستلی کاشف اکسیژن عنوان کرد. وی اولین کسی بود که قابلیت لاستیک در پاک کردن اثر مواد را مشاهده کرد. مواد لاستیکی تنها نتیجه تلاش در جهت تفلیحی و حفظ موادی چون افتیون ، بوتادیان و ایزوپرن بودند که از تقطیر تخریبی لاستیک طبیعی بدست میآمدند، بدین ترتیب راه تولید لاستیک سنتزی گشوده شد.
با آغاز جنگ جهانی اول ، انواع نامرغوب لاستیک از دی متیل بوتادیان در آلمان و روسیه تولید شد. گو دید با کشف پخت لاستیک توسط گوگرد در سال 1839 به شهرت رسید. این کشف مشکل چسبانکی طبیعی لاستیک را حل کرد و آن را به صورت تجاری در آورد. بیشترین تغییرات به لحاظ تاریخی نتیجه محدودیت واردات لاستیک طبیعی به آمریکا بر اثر تهاجم نیروهای ژاپنی در سال 1941 بوده است. این حرکت سبب پژوهش و ساخت انواع لاستیکهای سنتزی طی سالهای بعد شد.
منابع لاستیک طبیعی (کائوچو)
گیاهان بیشماری از جمله قاصدک ، گوایل ، گل روبینه و توت آمریکایی به عنوان منبع لاستیک پیشنهاد شده بودند. ولی هیچ یک توفیق درخت شیرابه ساز هوآ برزیلینسیس و همچنین صمغ درخت ساپوریلا و درخت بالاتا را نداشته است. لاستیک طبیعی عمدتا در کشتزارهای مالزی ، اندونزی ، لیبریا و همساگیانثی تولید شد، احتمالا به این علت که آنها مشکل بیماریهای قارچی و حشرات را که کشتزاهای بومی در آمریکا را تهدید میکرد نداشتند. حدود 7 سال زمان لازم است تا این درختان به سن باروری برسند و پس از آن به مدت چند سال بار میدهند. بهره باردهی در طول جنگ دوم افزایش یافت و در حال حاضر از کشف انواع اصلاح شده درخت ، بهرهای بیش از 3000 کیلوگرم در هکتار (در سال) بدست میآید.
ساختار لاستیک طبیعی
لاستیک طبیعی یا کائوچو ، سیس- 1 ، 4- پلی ایزوپرن است و مولکولهای آن بر اثر کشش ، بلوری میشوند، بدین ترتیب شکل مطلوبی از تقویت حاصل میشود. به عنوان پیش نیاز ساختاری ، مولکولهای لاستیکهای طبیعی و سنتزی باید طویل باشند. خاصیت مشخصه کشیدگی برگشتپذیر به دلیل ترتیب اتفاقی و کلافی زنجیرهای بلند بسپاری است. بر اثر کشش ، زنجیرها بهم میخورند ولی مثل یک فلز ، پس از رها کردن تنش به شکل کلافی خود بر می گردند. لاستیک طبیعی 6 تا 8 درصد مواد غیر پلاستیکی دارد و در برابر گرما اندوزی مقاومت زیادی نشان میدهد.
روش تهیه لاستیک طبیعی
برای بدست آوردن شیرابه ، پوست درخت را طوری برمیدارند که مایع در فنجانهای کوچکی جمع شود، فنجانها باید مرتبا جمعآوری شوند تا از گندیدگی یا آلودگی شیرابه جلوگیری شود. پس از آن شیرابه به محل جمع آوری برده میشود و در آنجا پس از صاف شدن با افزودن آمونیاک محافظت میشود. لاستیک از طریق فرآیندی موسوم به انعقاد جدا میشود. این کار با افزودن اسیدها یا نمکهای مختلف انجام می گیرد. در طی این عمل ، لاستیک به شکل یک توده سفید خمیری از مایع جدا می شود، و سپس از آن با استفاده از غلتک ورقهای و در نهایت خشک می گردد.
روش جدیدتر این است که با استفاده تیغههای دوار یا اعمال برش بین دو غلتکی که با سرعت متفاوت می چرخند ، شیرابه منعقد شده را به دانه تبدیل میکنند. دانهها سپس به مدت چند ساعت در خشک کنهای مکانیکی خشک میشوند، این عمل در روش قدیمی که از هوا یا دود چوب برای خشک کردن استفاده می شد چندین روز به طول میانجامید. به هر صورت ورقه یا دانه خشک شده متراکم و از آن مدلهایی به وزن 33 کیلوگرم می سازند.
مقداری از لاستیک طبیعی بصورت شیرابه به بازار عرضه میشود. پیش از آنکه لاستیک را بتوان با انواع افزودنیهای لازم آمیزه کاری مثل دوده (به عنوان پرکن) گوگرد یا ترکیبات گوگردی ، تسریع کننده و ولکانش ، ضد اکسنده محافظ و روغن بر روی همان غلتکها یا مخلوطکن ممکن است به ارتفاع یک ساختمان دو طبقه باشد و در عین حال تنها مقدار کمی لاستیک را در یک زمان میتوانند عمل آورند. یک نمونه مخلوطکن ممکن است به ارتفاع یک ساختمان دو طبقه باشد و در عین حال تنها بستههای 250 کیلوگرمی را جوابگو باشد. پس از اختلاط ، لاستیک با روزن رانی یا قالب گیری به شکل محصول دلخواه در می آید و بعد پخت می شود. و ولکانشی به یک پلیمر سخت شبکهای میانجامد که با گرمادهی مجدد نرم و با ذوب نمیشود.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 263 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:47
تاریخچه
از نظر قدمت تاریخی برای صنایع لاستیک منشا دقیقی نیست. اما اعنقاد این است که بومیان آمریکای مرکزی از برخی از درختان شیرابههایی استخراج میکردند که این شیرابهها که بعدها نام " لاتکس" را بخود گرفت اولین مواد لاستیکی را تشکیل میدادند.
پدیده ولکانیزاسیون
در سال 1829 ، "گودییر" از آمریکا و "مکین تاش" از انگلستان ، این دو متوجه شدهاند که در اصل مخلوط کردن لاتکس طبیعی با سولفور و حرارت دادن آن، مادهای قابل ذوب و قابل شکل دادن ایجاد میشود که میتوان از آن، محصولات مختلفی از قبیل چرخ ارابه یا توپ تهیه کرد.
این پدیده همان پدیده ولکانیزاسیون است که در طی آن لاستیک اکسیده میشود و سولفور کاهیده و به سولفید تبدیل میشود. البته این عمل در دمای 110 درجه سانتیگراد تهیه می شود. نتیجه این کشف تولید مواد لاستیکی مثل لاستیکهای توپر، پوتین و ... است.
کائوچوی طبیعی و مصنوعی
کائوچوی طبیعی در شیره درختی به نام هوا ، Hevea وجود دارد و از پلیمر شدن هیدروکربنی به نام 2- متیل- 1 و 3- بوتادین معروف به ایزوپرن بوجود میآید. با توجه باینکه در فرمول ساختمانی کائوچو یا لاتکس طبیعی هنوز یک پیوند دوگانه وجود دارد، به همین دلیل وقتی کائوچو را با گوگرد یا سولفور حرارت دهیم، این منومرها ، پیوند پی را باز میکنند و با ظرفیت های آزاد شده ، اتم گوگرد را میگیرند. در نتیجه کائوچو به لاستیک تبدیل میگردد.
حرارت دادن کائوچو با گوگرد و تولید لاستیک را اصطلاحا ولکانیزاسیون Vulcanizataion مینامند. به همین دلیل، لاستیک حاصل را نیز، "کائوچوی ولکانیزه" گویند. چند نوعی کائوچوی مصنوعی نیز ساخته شدهاند که از مواردی مانند 1 و 3- بوتادی ان و جسمی به نام 2- کلرو- 1 و 3- بوتادین معروف به "کلروپرن" و جسم دیگری به فرمول 2 و 3- دی متیل- 1 و 3- بوتادین بتنهایی یا مخلوط درست شدهاند. کلروپرن به راحتی پلیمریزه شده و به نوعی کائوچوی مصنوعی به نام "نئوپرن" تبدیل میشود.
تکامل در صنعت لاستیک
بعدها در سال 1888 خواص مکانیکی لاستیکهای تهیه شده توسط گودییر و مکین تاش با استفاده از کربن سیاه به عنوان یک ماده پرکننده و افزودنی بسیار بهبود بخشیده شده و در نتیجه لاستیکهای بادی دانلوب ، "تیوپ" تهیه شد. بعد از آن لاستیکهای سنتزی تهیه و به بازار عرضه شد مانند ایزوپرن ، بوتادی ان و لاستیکهای تیوکل.
بعدها لاستیکهای سنتزی مثل کوپلیمرهای استیرن و بوتادیان تهیه شد که در سال 1941 مصرف آن صفر بود. اما در سال 1945 مصرف آن 700000000 میرسید. به موازاتی که مصرف لاستیکهای سنتزی بالا میرود، مصرف لاستیکهای طبیعی پایین میآید. چون لاستیکهای سنتزی اقتصادیتر هستند.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 418 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:45
امروزه به موازات استفاده از رنگهای مصنوعی و توسعه صنعت رنگ سازی ، صنعت رنگرزی (dying industry) نیز در میدان بسیار وسیعی عمل مینماید و این کار با استفاده از پیشرفتهترین تکنولوژی و بکارگیری دستگاههای جدید و خود کار انجام میپذیرد. رنگرزی روی منسوجات بر اساس نفوذ و جذب سطحی انجام میگیرد. بنابراین برای درک چگونگی آن بایستی چگونگی جذب و تثبیت رنگ مواد و خواص فیزیکی و شیمیایی رنگها و غیره شناخته شود.
امروزه به موازات استفاده از رنگهای مصنوعی و توسعه صنعت رنگ سازی ، صنعت رنگرزی (dying industry) نیز در میدان بسیار وسیعی عمل مینماید و این کار با استفاده از پیشرفتهترین تکنولوژی و بکارگیری دستگاههای جدید و خود کار انجام میپذیرد. رنگرزی روی منسوجات بر اساس نفوذ و جذب سطحی انجام میگیرد. بنابراین برای درک چگونگی آن بایستی چگونگی جذب و تثبیت رنگ مواد و خواص فیزیکی و شیمیایی رنگها و غیره شناخته شود.
تاریخچه
برخی بر این عقیدهاند که رنگرزی در 3000 سال قبل از میلاد در چین رایج بود. ولی از 2500 سال قبل از میلاد ، آثار مکتوبی در مذاهب هندی بدست آمده است که نشان میدهد در آن زمان ابریشم و پارچههای زربافت را رنگآمیزی میکردند. صنایع رنگرزی احتمالا از طریق ایران به مصر منتقل شد.
در هر حال ، صنعت رنگرزی برای نخستین بار در سال 1371 میلادی در فلورانس ایتالیا شکل گرفت و در سال 1382 میلادی منسوخ شد. اما پس از مدت کوتاهی در سراسر اروپا مجددا پا گرفت. در سال 1371، اولین شرکت رنگ سازی یعنی کمپانی رشیب فول در انگلستان به ثبت رسید. کلیه رنگهایی که تا اواخر قرن نوزدهم در دسترس بودند، از منابع طبیعی استخراج میشدند. در سال 1856 ، "ویلیام پرکین" انگلیسی بطور تصادفی ، رنگ ارغوانی زیبایی را کشف کرد. بتدریج در فاصله چند سال ، رنگهای سنتزی آنیلین قرمز ، آبی ، سبز ، زرد ، سیاه ، نارنجی و قهوهای تهیه شد.
علت پیدایش رنگ در مواد
برخی از مواد شیمیایی وقتی که در مقابل نور سفید ( مرکب از هفت رنگ ) قرار میگیرند، بسته به ساختاری که دارند، طول موج معینی از نور را جذب میکنند و بقیه نور به رنگ الوان ( غیر از سفید ) ظاهر میشود. اگر چنین مولکولی به گونهای بتواند با الیاف مختلف ترکیب یا به آن متصل شود، موجب رنگی شدن آن الیاف میشود.
وجود گروهایی مانند نیترو ، نیتوزو ، آزو ، و کربونیل ، موجب بروز رنگ در مواد میشود. از این رو ، این گروهها را کروموفور مینامند. این ترکیبات رنگی ، علاوه بر گروههای کروموفور ، اگر با گروههای دیگری نظیر آمینو ، آمینوی استخلاف شده هیدروکسیل سولفنیک یا کربوکسیل که گروههای اگزوکروم نامیده میشود، همراه باشند، رنگهای مرغوبی را از نظر رنگرزی بوجود میآورند.
چگونگی تثبیت رنگ مواد
با در نظر گرفتن سه مرحله میتوان تثبیت رنگ روی الیاف را توجیه کرد:
انتقال مولکولهای رنگ در سطح الیاف بوسیله جذب
انتقال رنگ از سطح الیاف به مرکز آنها
تثبیت مولکولهای رنگ به کمک پیوند کووالانسی ، هیدروژنی و یا دیگر نیروهایی که ماهیت فیزیکی دارند.
تثبیت رنگ بر روی الیاف به سه عامل بستگی دارد که عبارتند از:
نیروی الکتریکی
همه الیاف ، وقتیکه در آب یا محلولهای آبی حل میشوند، دارای پتانسیل الکتریکی میشوند. الیاف سلولزی در محلولهای خنثی ، دارای بار منفیاند. اما الیاف پروتئینی وقتی که PH فاز آبی ، زیر نقطه ایزوالکتریک است، دارای بار مثبت و وقتی بالای نقطه ایزوالکتریک باشد، دارای بار منفیاند.
گرما
اکثر رنگها نیز بصورت متیلهای یونیاند که در برخورد با الیاف مذکور در سطح آن تثبیت میشوند. اگر بین یونهای رنگ و الیاف دافعه الکتریکی وجود داشته باشد، برای خنثی کردن آن و نزدیک کردن الیاف و مولکولهای رنگ به یکدیگر ، ارتعاش مولکولی را به کمک گرما افزایش میدهند بدین طریق ، با افزایش فعالیت ارتعاشی ، مولکولهای رنگ به الیاف نزدیک میشوند.
بهم زدن (نیروی مکانیکی)
بهم زدن ، وقتی مؤثر واقع میشود که مقادیر رنگ در محلول محدود باشد. در چنین شرایطی ، مبادله بین رنگ و سطح الیاف شدت مییابد. بدیهی است که هر چه اندازه مولکول رنگ کوچکتر باشد، این مبادله سریعتر انجام میگیرد.
نمونههای رنگهای طبیعی
نمونهای از رنگهایی که از منابع طبیعی استخراج میشدند:
رنگ آبی نیلی :از رنگ نیلی که از گیاهان بومی مصر است و در هند نیز میروید، استخراج میشد. این رنگ را وسمه نیز میگفتند.
رنگ قرمز ترکی یا آلیزارین :که از ریشه گیاهی به نام روناس بدست میآمد.
رنگ سیاه :از درخت بقم تهیه میشد.
رنگ ارغوانی :از نوعی ماهی فلس دار دریای مدیترانه بدست میآید که برای رنگ کردن لباس امپراتوری روم و غیره از آن استفاده میشد.
رنگ قرمز :از حشره قرمز دانه که بر روی برگ کاکتوس زندگی میکند، بدست میآمد.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 273 تاريخ : دوشنبه 15 تير 1388 ساعت: 21:41
آرشیو مطالب
- اسفند 1386
- مهر 1386
- آبان 1386
- دی 1387
- بهمن 1387
- اسفند 1387
- فروردين 1387
- خرداد 1387
- مهر 1387
- آبان 1387
- آذر 1387
- بهمن 1388
- اسفند 1388
- فروردين 1388
- ارديبهشت 1388
- خرداد 1388
- تير 1388
- شهريور 1388
- آبان 1388
- بهمن 1389
- اسفند 1389
- فروردين 1389
- ارديبهشت 1389
- خرداد 1389
- تير 1389
- شهريور 1389
- مهر 1389
- آبان 1389
- دی 1390
- بهمن 1390
- اسفند 1390
- فروردين 1390
- ارديبهشت 1390
- خرداد 1390
- مرداد 1390
- شهريور 1390
- مهر 1390
- آبان 1390
- آذر 1390
- دی 1391
- بهمن 1391
- اسفند 1391
- فروردين 1391
- ارديبهشت 1391
- تير 1391
- مرداد 1391
- شهريور 1391
- مهر 1391
- آبان 1391
- آذر 1391
- بهمن 1392
- اسفند 1392
- فروردين 1392
- تير 1392
- مرداد 1392
- شهريور 1392
- آبان 1392